Zdravo svima! Djevojke koje su bile u takvim situacijama, odgovore! 27. maja održan je prvi skrining. Ultrazvuk je bio sve normalan. Zabilježili su telefon za svaki slučaj, ali nisam očekivao da bi mogli nazvati, a sada tjedan dana poziv - vratite se u CPS, imate visok rizik. Ne sjećam se sebe, u suzama, stigao sam na pamučne noge, uzeo sam sve komade papira. Rizik 1:53. Sutradan sam otišao udvostručiti. Ultrazvuk je vrlo dugo pogledao želudac, a važan je da je doppler nekoliko puta uključio doplera, a sve se čini da je sve, ali nije se svidelo doplerometrije Truskidalnog ventila: regurgitaciju. Uneli su podatke o novom ultrazvuku u programu i probir rezultata sedmičnih ograničenja, računar je izdao rizik od SD 1: 6. Poslan u genetiku. Gledajući zaključak, objasnila mi je da bi ova regurgitacija mogla biti jednostavno obilježja ploda, ali na naknadu s podcjenjivim pokazateljem Papp-a - 0.232 mama, marker je hromozomalnih anomalija. Sve ostalo u normalnom rasponu. Predložili su da prolaze vršljana vrba za biopsiju. Još uvijek sam odbio, medicinska sestra je skoro pala sa stolice, poput rizika toliko visoka, a ha se ne liječe i na mom mjestu ne bi ni pomislila ni minut. Zainteresirani za genetiku o analizi panorame (strašno dragi gen. Analiza na majčinoj krvi), odgovorila mi je da bi to sigurno moglo učiniti, ali on isključuje samo 5 glavnih ha i nekoliko vrlo rijetkih, ne može u potpunosti isključiti anomalije, I u mom slučaju preporučuje se invazija. Već sam pročitao tonu članaka, pitanja i svega ovakvog na ovoj temi, a ne razumijem šta je tako strašno pronađeno u mojim analizama? Pogreškati kako se pokazalo kao fiziološka u ovom periodu i odvija se za 18-20 tjedana (ako ne govori o riziku od srčanih oštećenja, mnogi prolazi nakon porođaja, a neki ljudi žive s njom i ne utječu na bilo šta. Pogotovo U njenom mužu prolepi minalni ventil koji je dobio od mame, možda je nekako međusobno povezano). Hormoni možda uopće ne moraju biti indikativni, jer Prihvatio sam Duphaston od početka trudnoće, dva sata prelazim prije analize (ispada da ne možete jesti 4 sata prije, nisam rekao za to), popio sam kafu, nervozu i zabrinuta zbog ultrazvuka A krv se boji, a nedavno hronični umor, sa starijim djetetom, umoran sam. I sve to utiče na rezultate. Ništa poput genetičara nije postavljeno, nije me zainteresiran, oni tamo imaju neku vrstu transportera i činilo mi se da sam tamo gurnuo za statistiku. Ali jedina sumnja da su posadili u meni, odvezao sam se, brinuo sam se za godinu koja je pred nama. Muž ubedi biopsiju. Strašno se plašim posljedica, bojim se izgubiti ili naštetiti djetetu, posebno ako je zdrav. S jedne strane, ako je sve u redu, uzdahnite s olakšanjem i pošaljite sve doktore. S druge strane, ako je sve loše, šta da radim? Hoću li moći prekinuti trudnoću, dopustiti vašem djetetu u meni, pogotovo sada kad mi se čini, počinjem da osjetim. Ali druga opcija će moći podići takvo dijete koje je potreban poseban pristup i puno pažnje, kada ponekad želi pobjeći od prilično zdrave kćeri ... Prokletstvo, sve su mi se misli poslane. Ne znam kako biti ... Samo u slučaju da ću dati podatke o skriningu:
Termin b-: 13ned
Okupa srca 161 ICE / min
Venski kanal PI 1,160
Horion / sadnica niska na prednjem zidu
Pupovina 3 plovila
Anatomija fetusa: Sve je utvrđeno, sve je normalno
b-HGCH 1.091 mama
Papp-a 0.232 mama
Maternica pi 1.240 mama
Trisomija 21 1: 6
Trisomija 18 1: 311
Trisomija 13 1: 205
Preeklampsija do 34 sedmice 1: 529
Preeklampsija do 37 tjedana 1: 524
7.1. Klasifikacija dijabetesa
Dijabetes(SD) je grupa metaboličkih bolesti koje karakterišu hiperglikemija zbog kršenja izlučivanja i / ili efikasnosti inzulina. Hronična hiperglikemija, koja se razvija u SD-u, prati razvoj komplikacija mnogih organa i sistema, prije svega, od srca, krvnih žila, očiju, bubrega i živaca. Ukupno pati od 5-6% stanovništva. U ekonomski razvijenim zemljama svijeta svakih 10-15 godina, broj pacijenata sa CD-om povećava se za 2 puta. Životni vijek na CD-u smanjuje se za 10-15%.
Uzroci razvoja SD-a široko su varirani. U velikoj većini slučajeva CD-a, bilo zbog apsolutnog nedostatka inzulina (Tip 1 dijabetes -SD-1), ili zbog smanjenja osjetljivosti perifernih tkiva do inzulina u kombinaciji sa disfunkcijom tajna β-ćelija (Tip 2 dijabetes -SD-2). U nekim slučajevima, dodjela pacijenta na SD-1 ili SD-2 je ipak, ipak, kompenzacija CD-a je značajnija, a ne tačno uspostavljanje njegove vrste. Etiološka klasifikacija izdvaja četiri glavne kliničke klase SD (Tabela 7.1).
Najčešća SD-1 (klauzula 7.5), SD-2 (str. 7.6) i gestacijsko SD (klauzula 7.9) razgovaraju se u zasebnim poglavljima. Na ostale specifične vrstepostoji samo oko 1% slučajeva SD-a. Čini se da je etiologija i patogeneza ovih vrsta SD-a proučavala u odnosu na SD-1, a posebno SD-2. Brojne varijante SD-a nastaju zbog monogeničkog naslijeđenog genetski nedostaci funkcijeβ Boce.To uključuje različite mogućnosti za autosomno dominantni naslijeđeni mody sindrom (engleski. zrelost na katerovima za osnivanje mladih- Mladih za odrasle u mladim), koji karakteriše kršenje, ali ne i nedostatak sekrecije inzulina sa normalnom osjetljivošću na njemu periferna tkiva.
Stol. 7.1.Klasifikacija dijabetesa
Povremeno rijetko pronađen genetski nedostaci inzulinapriključena mutacija receptora inzulina (leprechaunism, sindrom stalak za stalak). CD se prirodno razvija sa bolesti exocian dela gušterače,dovodeći do uništavanja β-ćelija (pankreatitis, pancoratektomiju, cistična fibroza, hemokromatoza), kao i pod velikim brojem endokrinih bolesti, u kojima se pojavljuju prekomjerne proizvode kontinuiteta (akromegalija) (Acromegaly, sindrom za kontinuitet). Lijekovi i hemikalije(Vakor, pentamidin, nikotinska kiselina, diazoksid itd.) Rijetko su uzrok SD-a, ali može doprinijeti demonstraciji i dekompanziranju bolesti kod pojedinaca sa inzulinskim otporom. Red zarazne bolesti(Rubeola, citomegalija, koke i adenoviruška infekcija) mogu biti popraćena uništavanjem β ćelija, dok većina pacijenata definira imunogenetski markere SD-1. Do rijetki oblici imuno posredovanog dijabetesasD, razvijanje kod pacijenata sa "Čvrsti-Rnan" -Sindrom (autoimunom neurološkom bolešću), kao i dijabetes zbog efekata autoantiboda na insulinske receptore. Nalaze se različite varijante SD s povećanom frekvencijom na
mnogi genetski sindromi, posebno, u dolje sindromi, Klinfelter, Turner, Volfran, Prader-Willie i brojne druge.
7.2. Klinički aspekti metabolizma ugljikohidrata
Insulinsintetizira se i izlučuju β-ćelije otoka Langerhana gušterače (PJZ). Pored toga, otoci Langerhan se izlučuju glukagonu (α-ćelije), somatostatin (δ ćelije) i pankreatički polipeptid (pp ćelija). Hormoni otopljane ćelije djeluju jedni s drugima: Glukagon obično potiče sekreciju inzulina i somatostatin potiskuje izlučivanje inzulina i glukagona. Molekula inzulina sastoji se od dva polipeptidna lanca (lanac - 21 aminokiselina; u lancu - 30 aminokiselina) (Sl. 7.1). Inzulin sinteza započinje formiranjem Preprointulin, koji dijeli protease obrazovanja pROINSULIN.U sekretornim granulama stroja, Golgi, pinsulin se dijeli u inzulin i C-peptid,koji se oslobađaju u krv u procesu egzocitoze (Sl. 7.2).
Glavni stimulans sekrecije inzulina je glukoza. Oslobađanje inzulina kao odgovor na povećanje glukoze u krvi dvofazni(Sl. 7.3). Prva ili akutna faza traje nekoliko minuta, a povezan je s puštanjem nakupljanja
 Sl. 7.1.Dijagram primarne strukture molekula inzulina
Sl. 7.1.Dijagram primarne strukture molekula inzulina
 Sl. 7.2.Shema biosinteze inzulina
Sl. 7.2.Shema biosinteze inzulina
shegne u β-ćelijskoj inzulinu u periodu između obroka. Druga faza se nastavlja sve dok nivo glikemije ne doseže normalan trgovac (3,3-5,5 mmol / l). Slično tome, β-ćelije utječu na pripreme sulfonylurea.
Prema portalnom inzulinskom sustavu doseže jetra- Njegov glavni ciljni organ. Jetreni receptori vezuju polovinu izlučenog hormona. Još polovina, pala u sistemski krvotok, doseže mišiće i masni tkivo. Većina inzulina (80%) podvrgnuta je proteolitičkom propadanju u jetri, ostatak je u bubrezima, a samo se manji iznos metabolizira direktno sa mišićnim i masnim ćelijama. Norma pjz.
 Sl. 7.3.Dvofazni ispuštanje inzulina pod utjecajem glukoze
Sl. 7.3.Dvofazni ispuštanje inzulina pod utjecajem glukoze
odrasli muškarac izlučuje 35-50 jedinica dnevno, što je 0,6-1,2 jedinice na 1 kg tjelesne težine. Ova sekrecija podijeljena je u prehrambeni i bazalni. Izlučivanje hraneinsulin co konzultira postprandialnu dizanje glukoze, I.E. Zbog njega se osigurava neutralizacija hiperglimizacije hrane. Količina prehrambenih inzulina približno odgovara broju uzeta ugljikohidrata - oko 1-2,5
do 10-12 g ugljikohidrata (1 jedinica za hljeb - hee). Bazalni izlučivanje inzulinapruža optimalan nivo glikemije i anabolizma u intervalima između hrane i za vrijeme spavanja. Bazalni inzulin izlučuje brzinu od oko 1 UN / H, s dugoročnom vježbanjem ili dugom glatkom, značajno se smanjuje. Inzulin hrane čini najmanje 50-70% dnevne proizvodnje inzulina (Sl. 7.4).
Sekrecija inzulinama podložna je ne samo hrani, već i svakodnevno
 Sl. 7. .4.
Dnevna proizvodnja Insulin Norma
Sl. 7. .4.
Dnevna proizvodnja Insulin Norma
oscilacije:potreba za inzulinom raste u ranim jutarnjim satima, a u budućnosti postepeno padne tokom dana. Dakle, 2,0-2,5 tenisice izlučuju se za doručak na 1 hebu, za ručak - 1,0-1,5 jedinice, te za večeru - 1,0 jedinice. Jedan od razloga za takvu promjenu osjetljivosti na inzulinu je visok nivo niza konjunralnih hormona (prvenstveno kortizol) u jutarnjim satima, koji se postepeno padne na minimum na početku noći.
Osnovni fiziološki efekti Insulinpostoji stimulacija prijenosa glukoze kroz membrane ovisne o inzulinu. Glavna tijela inzulina su jetre, masni tkivo i mišić. U tkivima ovisno o inzulini, protok glukoze u koji ne ovisi o efektima inzulina, prvenstveno uključuju središnji i periferni nervni sistem, endotel krvnih žila, krvnih zrnaca itd. Izulinsku sintezu glikogena u jetri i mišići, sintezu masti u jetri i masnom tkivu, sinteza proteina u jetri, mišićima i drugim organima. Sve ove promjene usmjerene su na korištenje glukoze, što dovodi do smanjenja razine u krvi. Fiziološki antagonist inzulin je glucagonkoji potiče mobilizaciju glikogena i masti iz skladišta; Normalno, nivo glukagona mijenja recipročni inzulinski proizvodi.
Biološki efekti inzulina posreduju receptorikoji se nalaze na ciljnim ćelijama. Insulin receptor je glikoprotein koji se sastoji od četiri podjedinice. Sa visokim nivoom inzulina u krvi, smanjuje se broj njegovih receptora na principu niže regulative, što je popraćeno smanjenjem osjetljivosti ćelije na inzulin. Nakon vezivanja inzulina sa mobilnim receptorom, kompleks dolazi unutar ćelije. Sljedeći unutar mišićne i masne ćelije, inzulin uzrokuje mobilizaciju unutarćelijskih vezikula, koji sadrže glukozni transporterGlut-4. Kao rezultat toga, Vesticle se prelaze na površinu ćelije, gdje glup-4 vrši funkciju ulaza za glukozu. Sličan učinak na glut-4 ima fizički napor.
7.3. Laboratorijska dijagnostika i kriterijumi za nadoknadu dijabetesa
Laboratorijska dijagnostika SD-a temelji se na određivanju nivoa glukoze u krvi, dok su kriteriji za dijagnostiku ujedinjeni za sve
vrste i varijante SD (Tabela 7.2). Podaci drugih laboratorijskih studija (nivo glukosurije, definicija nivoa glickiranog hemoglobina) ne smiju se koristiti za provjeru dijagnoze dijagnoze. Dijagnoza SD-a može se postaviti na temelju dvokračnog otkrivanja jednog od tri kriterija:
1. Sa očiglednim simptomima SD-a (poliuria, polidipsija) i nivo glukoze u čvrstoj kapilarnoj krvi, više od 11,1 mmol / l, bez obzira na doba dana i prethodnih obroka.
2. Na nivou glukoze u čvrstoj kapilarnoj krvi, prazan stomak više od 6.1 mmol / l.
3. Na nivou glukoze u čvrstoj kapilarnoj krvi 2 sata nakon prijema 75 grama glukoze (oralni test ležaja glukoze) više od 11,1 mmol / l.
Stol. 7.2.Kriteriji za dijagnosticiranje dijabetesa
 Najvažniji i značajniji test u dijagnostici CD-a je odrediti nivo glikemije na prazan stomak (najmanje 8 sati post). U Ruskoj Federaciji nivo glikemije obično se procjenjuje u čvrstoj krvi. Mnoge se zemlje široko koriste za određivanje nivoa glukoze
Najvažniji i značajniji test u dijagnostici CD-a je odrediti nivo glikemije na prazan stomak (najmanje 8 sati post). U Ruskoj Federaciji nivo glikemije obično se procjenjuje u čvrstoj krvi. Mnoge se zemlje široko koriste za određivanje nivoa glukoze
u krvnoj plazmi. Oralni test brade glukoze(OGTT; Određivanje nivoa glukoze 2 sata nakon primjene unutar 75 grama glukoze raspušten u vodi) u tom pogledu, postoji manja vrijednost. Ipak, na osnovu OGTT-a se dijagnosticira kršenje tolerancije glukoze(NTG). NTH se dijagnosticira ako se nivo čvrstog kapilarnog krvi nije prekoračio 6.1 mmol / l, a 2 sata nakon tereta, glukoza je veća od 7,8 mmol / l, ali ispod 11,1 mmol / l. Druga utjelovljenje carbohidratske razmjene je prekršena glikemija u praznoj trgovini(NGN). Potonje se uspostavlja ako je nivo glikomije od pune kapilarne krvi u prazan stomak u rasponu od 5,6-6,0 mmol / l, a 2 sata nakon opterećenja s glukozom manjim od 7,8 mmol / l). NTG i NGNT trenutno su ujedinjeni po mandatu prediabetbudući da su obje kategorije pacijenata visoko visok rizik od manifestacije SD-a i razvoja dijabetičke makroaganipatije.
Da bi dijagnosticirali SD, nivo glikemije mora se odrediti standardnim laboratorijskim metodama. U interpretaciji pokazatelja glikomije treba se imati na umu da prazan nivo želučanja glukoze u čvrstoj venskoj krvi odgovara njegovom nivou u čvrstom kapilaru. Nakon prijema hrane ili ogtta, njegov nivo u venskoj krvi iznosi oko 1,1 mmol / l niže nego u kapilari. Sadržaj glukoze u plazmi iznosi oko 0,84 mmol / l veći nego u čvrstoj krvi. Kako bi se procijenila naknada i adekvatnost CD terapije, nivo glikemije procjenjuje se u kapilarnoj krvi pomoću prenosivog glukometarsami pacijenti, njihova rodbina ili medicinsko osoblje.
S bilo kojom vrstom dijabetesa, kao i značajnim opterećenjem glukoze može se razviti glukozuriašto je posljedica viška praga reapsorpcije glukoze iz primarnog urina. Prag rebsorpcije glukoze značajno varira varira (≈ 9-10 mmol / l). Kao zasebni pokazatelj glukosurije za dijagnozu SD-a ne treba se koristiti. Normalno, s izuzetkom slučajeva značajnih opterećenja hranom rafiniranih ugljenih hidrata, Glukosuria nije pronađena.
Proizvodi keton Tel(Aceton, acetoacetat, β-hidroksibutirati) značajno se pojačava u apsolutnom nedostatku inzulina. Kada se dekompenzacija, SD-1 može odrediti izraženo ketonuria(Istražuje testne trake koje se spuštaju u urinu). Jednostavno (Trace) Ketonuria može se odrediti u zdravim ljudima sa gladi i fermentiranom dijetom.
Važan laboratorijski pokazatelj koji se koristi za diferencijalnu dijagnozu vrsta SD-a, kao i identificirati formiranje nedostatka inzulina kod pacijenata sa SD-2, je nivo C-peptid.U pogledu nivoa C-peptida u krvi, nesporno je suditi o umetanju β-ćelija PJZ-a. Potonji proizvodi PROINSULIN iz koje se C-peptid cijeplje pre izlučivanja, što spada u krv u istim iznosima sa inzulinom. Inzulin je u jetri sa 50% kontaktiran u jetri i ima poluživot u perifernoj krvi oko 4 minute. C-peptid iz jetrene protok krvi nije uklanja i ima poluživot u krvi od oko 30 minuta. Pored toga, nije povezana sa ćelijskim receptorima na periferiji. Stoga je definicija nivoa C-peptida pouzdaniji je test za procjenu funkcije izolacijskog aparata. Razina C-peptida je najificalno ispitana na pozadinu uzoraka stimulacije (nakon jela ili primjene glukagona). Test je ne informativan ako se provodi na pozadini izrečene dekompenzacije SD-a, jer izražena hiperglikemija ima toksični učinak na β-ćelije (glukozoksičnost). Izulinska terapija za nekoliko prethodnih dana do testnih rezultata neće utjecati.
Glavni svrha liječenjasvaka vrsta CD-a je sprječavanje njegovih kasnih komplikacija, koje se mogu postići uz pozadinu stabilne nadoknade na brojnim parametrima (tablica 7.3). Glavni kriterij za kvalitetu naknade za metabolizam ugljikohidrata na CD-u je nivo glikozirani (glikozilirani) hemoglobin (HbA1c).Potonji je hemoglobin, nepoznato povezan s glukozom. U eritrocitima glukoze dolazi samostalno od inzulina, a glikozilacija hemoglobina je nepovratan proces, a njegova diploma je izravno proporcionalna koncentraciji glukoze s kojom je kontaktirala 120 dana svog postojanja. Mali dio hemoglobina je glikozilaran i normalan; Sa CD-om se može značajno povećati. Razina HbA1c, za razliku od nivoa glukoze, koja se stalno mijenja, integralno odražava glikemiju u posljednjih 3-4 mjeseca. S tim je intervalom koji se preporučuje nivo HbA1c za procjenu kompenzacije SD-a.
Hronična hiperglikemija udaljena je od jedinog faktora rizika za razvoj i napredovanje kasnih komplikacija SD-a. U vezi evaluacija kompenzacije SDna osnovu kompleksa
laboratorijske i instrumentalne metode istraživanja (Tabela 7.3). Pored pokazatelja koji karakterišu stanje metabolizma ugljikohidrata, najvažniji je nivo krvnog pritiska i lipidnog spektra krvi.
Stol. 7.3.Kriteriji za kompenzaciju šećerne dijabetes
 Pored gore navedenih kriterija kompenzacije, potreban je individualni pristup prilikom planiranja ciljeva tretmana CD-a. Verovatnoća razvoja i napredovanja kasnih komplikacija SD (posebno mikroaganipatije) povećava se s povećanjem u trajanju bolesti. Dakle, ako kod djece i mladih pacijenata u budućnosti može dostići nekoliko desetljeća, potrebno je postići optimalne pokazatelje glikomije, zatim kod pacijenata koji imaju CD očigledno u starije i starosti, krutu euglememičku naknadu, značajno Poboljšanje rizika od hipoglikemije, ne uvijek prikladno.
Pored gore navedenih kriterija kompenzacije, potreban je individualni pristup prilikom planiranja ciljeva tretmana CD-a. Verovatnoća razvoja i napredovanja kasnih komplikacija SD (posebno mikroaganipatije) povećava se s povećanjem u trajanju bolesti. Dakle, ako kod djece i mladih pacijenata u budućnosti može dostići nekoliko desetljeća, potrebno je postići optimalne pokazatelje glikomije, zatim kod pacijenata koji imaju CD očigledno u starije i starosti, krutu euglememičku naknadu, značajno Poboljšanje rizika od hipoglikemije, ne uvijek prikladno.
7.4. Pripravci za inzulin i inzulinske terapije
Pripravci inzulina su od vitalnog značaja za pacijente sa SD-1; Pored toga, oni primaju do 40% pacijenata sa SD-2. Zajedničko indikacije za imenovanje inzulinske terapije u SD,mnogi od kojih se zapravo preklapaju jedno drugo uključuju:
1. Dijabetes tipa 1
2. Panketektomija
3. Ketoacidotsko i hiperosmolarno komi
4. Sa dijabetesom mellitus tip 2:
Eksplicitni znakovi nedostatka inzulina, poput progresivnosti tjelesne težine i ketoze, izražene hiperglikemije;
Velike hirurške intervencije;
Akutne makro-komplikovane komplikacije (moždani udar, infarkt miokarda, gangrene itd.) I jake zarazne bolesti, praćene dekompenzacijama metabolizma ugljikohidrata;
Nivo glikemije je prazan stomak više od 15-18 mmol / l;
Nedostatak plaćanja naknade, uprkos propisivanju maksimalnih dnevnih doza različitih tabletih saharhinjskih droga;
Kasne faze kasnih komplikacija SD-a (teške polineuuropatije i retinopatiju, hronični zatajenje bubrega).
5. Nemogućnost nadoknade gestacijskog dijabetesa pomoću prehrane i terapije.
Po porijeklupripravci inzulina mogu se svrstati u tri grupe:
Životinjski insulini (svinjetina);
Ljudski insulini (polu-sintetički, genetski inženjering);
Analozi inzulina (Lizpro, aspart, Glargin, Demide).
Napredak tehnologija za proizvodnju ljudskih insulina doveo je do upotrebe svinjski insulin(Različite od ljudske aminokiseline) nedavno se značajno smanjilo. Svinjski insulin može se koristiti za proizvodnju ljudskih inzulina polu-sintetička metodašto podrazumijeva zamjenu jedne različite aminokiseline u svojoj molekuli. Najviši kvalitet je različit genetski inženjeringljudski insulini. Da biste ih dobili, čovekovo mjesto genoma odgovornog za sintezu inzulina povezano je sa genom E.COLI.ili kultura kvasce, kao rezultat čija posljednja počinje proizvoditi ljudski inzulin. Stvorenje analogci Insulinuz pomoć permutacija različitih aminokiselina, svrha dobijanja lijekova s \u200b\u200bdatim i najpovoljnijim farmakokinetikom. Dakle, insulin lizpro (humalog) je analogni
inzulin akcije ultrašorta, dok se njegov efekti saharcinga razvija nakon 15 minuta nakon ubrizgavanja. Analog Glargin Insulina (Lantus), naprotiv, karakteriše dugačka akcija koja se nastavlja tokom dana, dok je karakteristika kinetike droge nedostatak izraženih vrhova koncentracije plazme. Većina trenutno korištenih inzulinskih preparata i njegovi analozi se proizvodi u koncentracija100 U / ml. Od trajanje akcijeinzuline su podijeljeni u 4 glavne grupe (Tabela 7.4):
Stol. 7.4.Farmakokinetika lijekova i inzulinskih analoga
 1.
UltraShort akcija (Lizpro, aspart).
1.
UltraShort akcija (Lizpro, aspart).
2. Kratka akcija (jednostavan ljudski inzulin).
3. Prosječno trajanje akcije (insulini na neutralnom protaminu Hagedorn).
4. Dugoročna akcija (Glagragin, Detech).
5. Mješavine inzulina raznih trajanja akcije (Novomix-30, humulin-MH, humalog mix-25).
Pripreme ultraShort akcija[Lizpro (Humalog), Aspart (Novorad)] su analogni inzulina. Njihove su prednosti brzi razvoj efekta šećera nakon ubrizgavanja (nakon 15 minuta), što vam omogućava da ubrizgavate odmah prije jela ili čak neposredno nakon jela (manje od 3 sata) , što smanjuje rizik od hipoglikemije. Pripreme kratka akcija(Jednostavan inzulin, insulin-redovan) je rješenje koje sadrži inzulin u koncentraciji 100 jedinica / ml. Injekcija jednostavnog inzulina napravljena je 30 minuta prije jela; Trajanje akcije je oko 4-6 sati. Pripravci ultra vijaka i kratkih radnji mogu se dati supkutano, intramuskularno i intravenski.
Među drogama prosječno trajanje akcijenajčešće se priprema koriste na neutralnom protaminu Hagedorn (NPH). Nph je protein koji je nepoznati adsorb insulin, usporavajući njezinu usisavanje iz potkožnog skladišta. Efektivno trajanje akcije Nph Insulina obično je oko 12 sati; Unose se samo supkutano. Insulin Nph je suspenzija, u vezi s tim, za razliku od jednostavnog inzulina u bočici, blatnjava, i sa dugom stojenjem postoji suspenzija, koja se mora temeljito miješati prije ubrizgavanja. Insulini Nph Za razliku od drugih priprema dužeg djelovanja mogu se miješati sa kratkim dječjim inzulinom (jednostavnim inzulinom), dok se farmakokinetika komponenti smjese neće promijeniti, jer NPH neće vezati dodatne količine jednostavnog inzulina (Sl. 7.5). Pored toga, protamin se koristi za pripremu standardnih mješavina inzulinskih analoga (Novomix-30, humalog-mix-25).
Među lijekovima dugoročne radnje trenutno aktivno koriste analoge inzulina glargin(Lantus) i determerary(Leewemir). Povoljna karakteristika farmakokinetike ovih droga je da, za razliku od inzulina NPC-a, oni pružaju uniformu i dugoročni protok lijeka iz potkožnog skladišta. S tim u vezi, Glargin se može imenovati samo jednom dnevno, dok gotovo nikakvo bez obzira na vrijeme dana.
 Sl. 7.5.Farmakokokokinetika različitih inzulinskih preparata:
Sl. 7.5.Farmakokokokinetika različitih inzulinskih preparata:
a) monokomponenta; b) Standardne inzulinske smjese
Pored monokomponentnih droga Inzulin, klinička praksa se široko koriste standardne smjese.U pravilu govorimo o kratkim ili ultrashort inzulinskim mješavinama sa inzulinom prosječnog trajanja akcije. Na primjer, lijek "Humulin-MW" sadrži u jednoj boci od 30% jednostavnog inzulina i 70% inzulin nph; Lijek "Novomiks-30" sadrži 30% inzulinskog asparta i 70% kristalnog protamina suspenzije inzulinskog asparta; Lijek "HUMALOG-MIX-25" sadrži 25% inzulin lispro i 75% obustave proučavanja inzulina zakupa. Prednost
standardne mješavine inzulina zamjena su dvije injekcije jedne i nekoliko velikih tačnosti komponenti smjese; Nemoguće je nemogućnost pojedinačnog doziranja pojedinih komponenti smjese. Ovo određuje sklonost upotrebe standardnih inzulinskih mješavina za CD-2 terapiju ili sa takozvanim tradicionalna terapija inzulinom(Imenovanje fiksnih doza inzulina), dok za intenzivna terapija inzulinom(Odabir fleksibilne doze ovisno o pokazateljima glikemije i količini ugljikohidrata u hrani poželjniji je za korištenje monokomponentnih lijekova.
Ključ uspješne inzulin terapije je jasno poštivanje tehnike ubrizgavanja.Postoji nekoliko načina za uvođenje inzulina. Najlakši i najlakšiji pouzdani način - ubrizgavanje sa inzulinom Špric.Pogodniji način uvođenja inzulina su injekcije pomoću ručice sa špricamakoji je kombinirani uređaj koji sadrži rezervoar za inzulin (uložak), dozirnog sistema i igle za injektora.
Za prateću terapiju (kada je u pitanju izrečena dekompenzacija SD ili o kritičnim državama), inzulin se uvodi supkutano. Injekcija inzulina kraće akcije preporučuje se u subkutano masno tkivo trbuha, inzulin duže djelovanja - u vlaknu kuka ili ramena (Sl. 7.6 a). Injekcije su duboko u subkutano tkivo kroz široko komprimiranu kožu pod uglom od 45 ° (Sl. 7.6 b). Pacijent treba preporučiti dnevnu promjenu mjesta za ubrizgavanje inzulina unutar istog područja kako bi se spriječio razvoj lipodstrofa.
Do Čimbenici koji utječu na brzinu apsorpcije inzulinaiz potkožnog skladišta treba pripisati dozu inzulina (povećanja doze), mjesto za ubrizgavanje (apsorpcija je brže od trbušnog vlakana), temperatura okoline (grijanje i masaža mjesta ubrizgavanja ubrzava apsorpciju ).
Složenija metoda administracije koja ipak, u mnogim pacijentima omogućuje vam da postignete dobre rezultate liječenja, je li upotreba izulin dispenzerili sistemi za kontinuirano potkožno insulinska administracija. Dispenzer je prenosivi uređaj koji se sastoji od računara koji postavlja režim opskrbe inzulinom, kao i inzulinski opskrbni sustav, izveden na kateteru i minijaturnu iglu u potkožnu
 Sl. 7.6.Injekcije ubrizgavanja: a) Tipična mjesta za ubrizgavanje; b) položaj igle inzulinske šprice tokom ubrizgavanja
Sl. 7.6.Injekcije ubrizgavanja: a) Tipična mjesta za ubrizgavanje; b) položaj igle inzulinske šprice tokom ubrizgavanja
masno tkivo. Uz pomoć raspršivača, vrši se kontinuirano bazalno uvođenje kratkog ili ultrašorta inzulina (stopa oko 0,5-1 E / sat), a prije uzimanja hrane, ovisno o sadržaju ugljikohidrata i nivoa glikemije, Pacijent uvodi potrebnu dozu bolusa istog inzulina kratke akcije. Prednost inzulinske terapije uz pomoć dispenzatora je uvođenje inzulina kratkog (ili čak ultrašorta) akcije, što je samo po sebi nešto fiziološki, jer je apsorpcija produženih inzulinskog preparata izložena velikim fluktuacijama; S tim u vezi, kontinuirano uvođenje kratkog akcijskog inzulina ispostavilo se kao postupci. Nedostatak inzulinske terapije uz pomoć dispenzatora je potreba za stalnim uređajem za nošenje, kao i dugoročni temelj igle za ubrizgavanje u potkožno tkivo, za koje zahtijeva periodičnu kontrolu nad procesom opskrbe inzulinama. Izulinska terapija uz pomoć dispenzatora prvenstveno se prikazuje pacijentima sa SD-1, koji su spremni savladati tehniku \u200b\u200bnjegovog održavanja. Pogotovo u vezi s tim trebalo bi obratiti pažnju na pacijente s izraženim fenomenom "jutarnje zore", kao i za trudnice i planiranje trudnoće pacijenata sa SD-1 i Parizom
s poremeženim načinom života (mogućnost fleksibilnijeg načina napajanja).
7.5. Dijabetes tipa 1
SD-1 - specifičan za organu autoimunebolest koja vodi do uništavanja proizvodnje inzulina β-ćelija PJZ otočića, manifestuju apsolutnim nedostatkom inzulina. U nekim slučajevima pacijenti sa eksplicitnim SD-1 nedostaju autoimune lizije markera β-ćelija (idiopatski SD-1).
Etiologija
SD-1 je bolest sa nasljednom predispozicijom, ali njegov doprinos razvoju bolesti je mali (određuje njegov razvoj za oko 1 / s). Koncentracija blizana jednim osobama na SD-1 iznosi samo 36%. Verovatnoća razvoja SD-1 u detetu sa bolesnom majkom je 1-2%, otac - 3-6%, brat ili sestra - 6%. Neki ili nekoliko humoralnih markera za autoimune lezije β-ćelija, na koje antitijele uključuju antitijela za PJZ, antitela za glutamate Decarboxylase (GAD65) i antitijela u tirozin fosfatazu (IA-2 i ια-2β) nalaze se u 85-90% pacijenata.. Ipak, faktori imuniteta ćelija priloženi su uništavanju β ćelija. SD-1 je povezan sa HLA Haplotipovima kao što su DQA.i DQB,istovremeno sam alel HLA-DR / DQmogu se predići razvoju bolesti, dok su drugi protestirani. Uz veću frekvenciju SD-1, u kombinaciji s drugim autoimunim endokrinima (autoimunim tiroiditisom, dodavanjem bolesti) i bolesti ne alkohola, poput alopecije, vitiliga, krunske bolesti, reumatske bolesti (Tabela 7.5).
Patogeneza
SD-1 se manifestuje tokom uništavanja autoimunog procesa 80-90% β-ćelija. Brzina i intenzitet ovog procesa mogu se značajno razlikovati. Najčešće tipičan protokbolesti kod djece i mladih Ovaj postupak se nastavljaju prilično brzo, nakon čega slijedi nasilna manifestacija bolesti, u kojoj se pojavi prvih kliničkih simptoma na razvoj ketoacidoze (do ketoacidotske kome) može proći samo nekoliko tjedana.
Stol. 7.5.Dijabetes tipa 1
 Nastavak tablice. 7.5.
Nastavak tablice. 7.5.
 Drugi, značajno rijetki slučajevi, u pravilu, u odraslih starim od 40 godina, bolest može teći latentne (Latentni autoimuni dijabetes odrasli - Lada),istovremeno, u debi bolesti, takvi pacijenti često uspostavlja dijagnozu SD-2, a tokom nekoliko godina, CD kompenzacija može se postići imenovanjem sumponfylurea lekova. Ali u budućnosti, obično 3 godine kasnije, postoje znakovi apsolutnog nedostatka inzulina (gubitak kilograma, Ketonuria, izražena hiperglikemija, uprkos prijemu tabletih lijekova saharbingama).
Drugi, značajno rijetki slučajevi, u pravilu, u odraslih starim od 40 godina, bolest može teći latentne (Latentni autoimuni dijabetes odrasli - Lada),istovremeno, u debi bolesti, takvi pacijenti često uspostavlja dijagnozu SD-2, a tokom nekoliko godina, CD kompenzacija može se postići imenovanjem sumponfylurea lekova. Ali u budućnosti, obično 3 godine kasnije, postoje znakovi apsolutnog nedostatka inzulina (gubitak kilograma, Ketonuria, izražena hiperglikemija, uprkos prijemu tabletih lijekova saharbingama).
Osnova patogeneze SD-1, kako je naznačeno, je apsolutni nedostatak inzulina. Nemogućnost ulaska u glukoze u tkanini ovisi o inzulinu (masnoća i mišića) dovodi do nestanka energije što rezultira intenziviranim lipolizom i proteolizom, s kojima je povezan gubitak tjelesne težine. Povećanje nivoa glikemije izaziva hiperalnost koja prati osmotski diureza i izražena dehidracija. U uvjetima nedostatka inzulina i neuspjeha energije razvijaju se konjurantni hormonski proizvodi (glukagon, kortizol, hormon rasta, koji, uprkos povećanju glikemije, određuje stimulaciju glukegeneze. Povećanje lipolize u adipoznom tkivu dovodi do značajnog povećanja koncentracije besplatnih masnih kiselina. Sa nedostatkom inzulina, liposintetska sposobnost jetre je potisnu i
masne kiseline počinju se uključiti u ketogenezu. Akumulacija ketonskih tijela dovodi do razvoja dijabetičke ketoze, a u budućnosti - ketoacidoza. Uz progresivno povećanje dehidracije i acidoze, delovanje se razvija komatozni (vidi stavak 7.7.1), koji, u nedostatku inzulin terapije i rehidracije, neminovno se završava smrću.
Epidemiologija
Na SD-1 postoji oko 1,5-2% svih slučajeva dijabetesa, a ova relativna figura nastavit će se smanjiti zbog brzog rasta incidencije SD-2. Rizik od razvoja SD-1 u cijelom životu predstavnika bijele rase je oko 0,4%. Incidencija SD-1 povećava se za 3% godišnje: za 1,5% zbog novih slučajeva i još 1,5% zbog povećanja životnog vijeka pacijenata. Prevalencija SD-1 varira ovisno o etničkom sastavu stanovništva. Za 2000. godinu iznosila je 0,02% u Africi, 0,1% u Južnoj Aziji, kao i u južnoj i centralnoj Americi i 0,2% u Evropi i Severnoj Americi. Najviša incidencija SD-1 u Finskoj i Švedskoj (30-35 slučajeva na 100 hiljada stanovnika godišnje), a najniža u Japanu, Kini i Koreji (respektivno 0,5-2,0 slučajeva). Vrhunski vrh povezano manifestacijom SD-1 odgovara oko 10-13 godina. U velikoj većini slučajeva, SD-1 se manifestuje do 40 godina.
Kliničke manifestacije
U tipični slučajevipogotovo kod djece i mladih, SD-1 deduje svijetlu kliničku sliku, koja se razvija nekoliko mjeseci ili čak sedmice. Manifestacija SD-1 može izazvati zarazne i druge istodobne bolesti. Karakterističan zajedničko za sve vrste simptoma SD-a,povezano sa hiperglikemijom: Polidipsija, Poliurija, Skin svrbež, ali u SD-1 su vrlo izraženi. Dakle, tokom dana pacijenti mogu piti i izvlačiti do 5-10 litara tekućine. Specifičnoza SD-1, simptom, koji je zbog apsolutnog nedostatka inzulina, gubitak kilograma, dosežući 10-15 kg za 1-2 mjeseca. Karakterizira ga teška opća i mišićava slabost, smanjene performanse, pospanost. Na početku bolesti neki se pacijenti mogu pojaviti povećanje apetita, koji zamjenjuje anoreksijom jer se razvija ketoacidoza. Potonje karakteriše izgled mirisa acetona (ili voćnog mirisa) iz usta, tosh-a
nota, povraćanje, često bol u stomaku (pseudoperitonite), teška dehidratacija i završava razvojem stanja komatoze (vidi stav 7.7.1). U nekim slučajevima prva manifestacija SD-1 kod djece progresivan je poremećaj svijesti do Komu protiv pozadine istodobnih bolesti, u pravilu, zarazne ili akutne hirurške patologije.
U relativno rijetkim slučajevima razvoja SD-1 u osobama od 35-40 godina (Latentni autoimuni dijabetes odraslih)bolest se može manifestirati ne tako svijetla (umjerena polikypsija i poliurija, nedostatak gubitka tjelesne težine), pa čak i otkrivaju slučajno s rutinskom definicijom nivoa glikemije. U tim slučajevima, pacijent često uspostavlja dijagnozu SD-2 i tabletih saharskih priprema (TSP) su propisane, što neko vrijeme pružaju prihvatljivu kompenzaciju CD-a. Ipak, nekoliko godina (često tokom godine) pacijent se pojavljuje simptomi uzrokovani rastućim apsolutnim deficitom inzulina: gubitak težine, nemogućnost održavanja normalne glikemije na pozadini TSP, ketoza, ketoacidoze.
Dijagnostika
S obzirom da SD-1 ima svijetlu kliničku sliku, a ujedno je i relativno rijetka bolest, definicija skrininga nivoa glikemije u cilju dijagnosticiranja SD-1 nije prikazana. Verovatnoća razvoja bolesti u blizini najbližeg rođaka pacijenata je niska, koja, zajedno sa nedostatkom efikasnih metoda primarne proprilakse, SD-1 određuje nepravisnost studije o imunogenetskim markerima bolesti. Dijagnoza SD-1 u velikoj većini zasniva se na identifikaciji značajne hiperglikemije kod pacijenata s teškim kliničkim manifestacijama apsolutnog nedostatka inzulina. Ogtt u svrhu dijagnostike SD-1 mora se izvesti vrlo rijetko.
Diferencijalna dijagnoza
U sumnjivim slučajevima (otkrivanje umjerene hiperglikemije u nedostatku eksplicitnih kliničkih manifestacija, manifestacije u relativno starcima), kao i u svrhu diferencijalne dijagnostike s drugim vrstama SD-a, koristi se za određivanje razine C-peptid(bazalni i 2 sata nakon obroka). Indirektna dijagnostička vrijednost u sumnjivim slučajevima može imati definiciju imunološki markeriSD-1 - antitijela za oralnu
PJZ, do glutamatdekarboksilaze (GAD65) i tirozin fosfataza (IA-2 i IA-2β). Diferencijalna dijagnoza SD-1 i SD-2 prikazana je u tablici. 7.6.
Stol. 7.6.Diferencijalna dijagnoza i razlike između SD-1 i SD-2
 Tretman
Tretman
Liječenje bilo koje vrste CD-a temelji se na tri osnovna načela: saharosyncing terapija (sa SD-1 - inzulinom terapijom), prehranom i obukom pacijenta. Inzulinoterapijana SD-1 nose zamjenaa njegov je cilj maksimalna imitacija fizioloških proizvoda hormona kako bi se postigli usvojeni kriteriji za naknadu (Tabela 7.3). Na fiziološkoj sekreciju inzulina je najpribliženije intenzivna terapija inzulinom.Potreba za inzulinom koja odgovara njoj bazalno izlučivanje,omogućuju ga dvije inzulinske injekcije prosječnog trajanja akcije (ujutro i navečer) ili jednu dugogodišnju injekciju inzulina (glargija). Ukupna doza bazalnog inso-
lina ne bi trebala prelazi polovinu cjelokupne dnevne potrebe za pripremom. Izlučivanje hrane ili bolusazamijenjena je injekcijama inzulina akcije kratke ili ultrašorta prije svakog unosa obroka, dok se njegova doza izračunava na osnovu količine ugljikohidrata, koji bi se trebao poduzeti tokom nadolazećeg unosa hrane i postojeći nivo Glikemija koju je pacijent odredio glukometom prije svake injekcije inzulina (Sl. 7.7).
Približan intenzivna shema terapije inzulina,što će se razlikovati gotovo svaki dan, može biti zastupljeno na sljedeći način. Oni nastaju od činjenice da je dnevna potreba za insulinom oko 0,5-0,7 jedinica na 1 kg tjelesne težine (za pacijenta s tjelesne težine od 70 kg oko 35-50 jedinica). Oko 1 / S - 1/2 ove doze bit će inzulin duže djelovanja (20-25 jedinica), 1/2 - 2 / s inzulinom kratke ili ultrastrum akcije. Doza inzulina Nph podijeljena je u 2 injekcije: ujutro 2 / s svoje doze (12 jedinica), u večernjim satima - 1 / s (8-10 jedinica).
Svrha prva fazabrtvljenje inzulinske terapije je normalizacija nivoa glukoze na prazan stomak. Večernja doza inzulina NPH-a obično se unosi u 22-23 sata, zajedno sa ubrizgavanjem kratkih akcija inzulina ispred doručka. Prilikom odabira večernje doze inzulina NPH-a potrebno je imati na umu mogućnost razvoja broja
 Sl. 7.7.Shema intenzivne inzulin terapije
Sl. 7.7.Shema intenzivne inzulin terapije
sasvim tipične pojave. Uzrok jutarnje hiperglikemije može biti nedovoljna doza produženih akcija inzulina, jer ujutro treba značajno povećavati potrebu za inzulinom ("Jutarnja zora" fenomen).Pored nedostatka doze, njegov višak može dovesti do jutarnje hiperglikemije. fenomen Somoga(Somogyi), postgoglikemijska hiperglikemija. Ovaj fenomen je objasnjen činjenicom da je maksimalna osjetljivost tkiva na inzulin označena između 2 i 4 sata noći. Trenutno je razina osnovnih konjunralnih hormona (kortizola, hormona rasta itd.) Normalna. Ako je večernja doza inzulina produžene akcije pretjerana, tada se u ovom trenutku razvija hipoglikemija.Klinički se može manifestirati loš san sa noćnim snovima, nesvjesnim akcijama u snu, jutarnju glavobolju i kvar. Razvoj u ovom trenutku hipoglikemije uzrokuje značajnu kompenzacijsku kompenzacijsku kompenzacijsku emisiju i druge konjnurane hormone hiperglikemija u jutarnjem satu.Ako u ovoj situaciji ne smanjuje, već će povećati dozu produženog inzulina, uloženo uveče, noćni hipoglikemija i jutarnja hiperglikemija bit će pogoršana da će na kraju može dovesti do sindroma hroničnog inzulinskog sindroma (Somoga sindrom) , što je kombinacija gojaznosti s hroničnom dekompenzacijom SD, česte hipoglikemije i progresivne kasne komplikacije. Za dijagnozu fenomena Somoge potrebno je proučiti nivo glikemije oko 3 sata, što je sastavna komponenta izbora terapije inzulinom. Ako je pad u noćnom hipoglikemiji u pogledu razvoja noćnog hipoglikemije, praćena hiperglikemijom ujutro (fenomen jutarnje zore), pacijent treba preporučiti ranije rast (6-7 ujutro) , dok se inzulin predstavio preko noći i dalje održava normalan nivo glikemije.
Druga ubrizgavanje inzulinskog Nph obično se vrši prije doručka zajedno sa jutarnjem ubrizgavanjem inzulina kratke (ultrašort) akcije. U ovom slučaju doza je odabrana prvenstveno na osnovu nivoa glikemije ispred glavne dnevne obroke (ručak, večera); Pored toga, može ograničiti razvoj hipoglikemije u intervalima između obroka, na primjer, u podne, između doručka i ručka.
Sve doze inzulin produžena akcija(Glargin) se uvodi jednom dnevno, a ne u osnovi, u koje vrijeme. Kinetika
glargin insulini i detech povoljniji su u pogledu rizika od hipoglikemije, uključujući noć.
Kratka ili ultrašorta inzulina doza čak i u prvom pacijentu, destinacija inzulina ovisit će o količini ugljikohidrata koji se koriste (krušne jedinice) i nivoa glikemije prije injekcije. Uvjetno se na temelju svakodnevnog ritma sekrecije inzulinskog izlučivanja, oko 1/4 kratkih djelujućih inzulina (6-8 jedinica) daje na večeru, preostala doza otprilike jednako podijeljenih u doručak i ručak (10-12 jedinica). Što je viši početni nivo glikemije, to će se manje smanjiti od strane umećenog inzulina. Injekcija kratkog akcijskog akcije iznosi 30 minuta prije jela, ultrašort akcije neposredno prije jela ili čak odmah nakon jela. Adekvatnost doze za kratkotrajne inzuline procjenjuje se u pogledu glikemije 2 sata nakon obroka i prije sljedećeg obroka.
Da bi izračunali dozu inzulina intenzivne terapije inzulinama, dovoljno je brojanje broja x, na osnovu komponente ugljikohidrata. Istovremeno se ne uzimaju u obzir svi proizvode ugljikohidrata, već samo takozvani izračunati. Potonji uključuje krompir, žito proizvode, voće, tekuće mliječne mliječne i slatke proizvode. Proizvodi koji sadrže nedovoljne ugljevke (većina povrća) se ne uzimaju u obzir. Razvijene su posebne tablice razmjene, uz pomoć od kojih se izražava količinu ugljikohidrata u njenom, možete izračunati potrebnu dozu inzulina. Jedan XE odgovara 10-12 g ugljikohidrata (Tabela 10.7).
Nakon uzimanja hrane koja sadrži 1 x, nivo glikemije se povećava za 1,6-2,2 mmol / l, tj. Otprilike onoliko koliko se nivo glukoze smanjuje prilikom uvođenja 1 U. Insulina. Drugim riječima, na svakom hee sadržanom u hrani koja se planira jesti, mora se unaprijed uvesti (ovisno o doba dana) oko 1 jedinice inzulina. Pored toga, moramo snimiti rezultate samokontrole nivoa glikemije, koji se izvodi prije svake ubrizgavanja, a doba dana (oko 2 jedinice inzulina na 1 hebu ujutro i na ručku, 1 jedinice 1 x - za večeru). Dakle, ako se otkriva hiperglikemija, doza inzulina, izračunata u skladu s nadolazećim obrokom (u smislu broja XE), treba povećati i obrnuto, ako se otkriva hipoglikemija, inzulin se unosi manje.
Stol. 7.7.Ekvivalentna zamjena proizvoda koji čine 1 x
 Na primjer, ako pacijent bude 30 minuta do planirane večere koja sadrži 5 hehe, nivo glikemije je 7 mmol / l, mora se uvesti 1 jedinice u glikemiju da se smanji na normalan nivo: od 7 mmol / l 5 mmol / l. Pored toga, na prevlakom 5 x mora se uvesti 5 uzinulina. Stoga će pacijent u ovom slučaju uvesti 6 jedinica kratke ili ultrashort akcije.
Na primjer, ako pacijent bude 30 minuta do planirane večere koja sadrži 5 hehe, nivo glikemije je 7 mmol / l, mora se uvesti 1 jedinice u glikemiju da se smanji na normalan nivo: od 7 mmol / l 5 mmol / l. Pored toga, na prevlakom 5 x mora se uvesti 5 uzinulina. Stoga će pacijent u ovom slučaju uvesti 6 jedinica kratke ili ultrashort akcije.
Nakon manifestacije SD-1 i početka inzulinske terapije, već dugo vremena, potreba za inzulinom može biti mala i biti manja od 0,3-0,4 jedinice / kg. Ovo razdoblje je naznačeno kao faza remisije, ili "Medeni mesec".Nakon hiperglikemije i ketoacidoze, koji ugušiva se izlučuju za inzulin iznosi 10-15% sačuvanim β-ćelijama, kompenzacijom hormonalnih poremećaja u uvođenju insulina obnavlja funkciju ovih ćelija na temu minimalni nivo. Ovaj period se može nastaviti od nekoliko tjedana do nekoliko godina, ali na kraju, zbog autoimunog uništavanja preostalih β-ćelija, završava "medeni mjesec".
Dijetasa SD-1 u obučenim pacijentima koji posjeduju vještine samokontrole i izbor inzulinske doze, može se liberalizirati, tj. približavajući se besplatnom. Ako pacijent nema višak ili deficit tjelesne težine, dijeta mora biti
izokalorian. Glavna komponenta hrane na SD-1 je ugljikohidrati, koji bi trebali imati oko 65% dnevne kalorage. Prednost treba dati proizvode koji sadrže kompleks, polako usisni ugljikohidrate, kao i proizvode bogate hranom. Treba izbjegavati proizvode koji sadrže ugljikohidrate (brašno, slatko). Udio proteina treba smanjiti na 10-35%, što pomaže u smanjenju rizika od razvoja mikroaktipatije i udjela masti - do 25-35%, a granične masti trebaju iznositi do 7% kalorative , što smanjuje rizik od ateroskleroze. Pored toga, potrebno je izbjeći uzimanje alkoholnih pića, posebno jakih.
Sastavna komponenta rada sa pacijentom sa SD-1 i zalogom svoje efektivne kompenzacije je obuka pacijenata.Kroz život pacijent mora svakodnevno ne samostalno ovisiti o brojnim faktorima za promjenu doze inzulina. Očito, zahtijeva posjedovanje određenih vještina koje pacijent treba obučiti. "Škola pacijenta SD-1" organiziran je u endokrinološkim bolnicama ili ambulantnim i predstavlja 5-7 strukturiranih klasa, na kojima je ljekar ili posebno obučena medicinska sestra u interaktivnom režimu koristeći principe treninga o raznim vizualnim pogodnostima selfontrol.
Prognoza
U nedostatku terapije inzulinom, pacijent SD-1 neminovno umire od ketoacidotske kome. Uz neadekvatnu terapiju inzulinom, na osnovu porijekla ne postoje kriteriji za kompenzaciju CD-a i pacijent je u stanju hronične hiperglikemije (Tabela 7.3), kasne komplikacije (§ 7.8) počinju razvijati i napredovati. Sa SD-1, najveći klinički značaj u tom pogledu ima manifestacije dijabetičkog mikroda (nefropatije i retinopatije) i neuropatije (sindrom dijabetičkog stopala). Makroaganipatija sa SD-1 na prvom planu relativno je rijetka.
7.6. Dijabetes tipa 2
Dijabetes tipa 2- hronična bolest manifestira kršenje berza ugljikohidrata sa razvojem hiperglikemije zbog inzulinskog otpora i sekretarne β-ćelijske disfunkcije,
kao i lipidni metabolizam s razvojem ateroskleroze. Budući da su glavni uzrok smrti i invalidnosti pacijenata komplikacije sistemske ateroskleroze, SD-2 se ponekad naziva kardiovaskularna bolest.
Stol. 7.8.Dijabetes tipa 2
 Etiologija
Etiologija
SD-2 je multifaktorijalna bolest sa nasljednom predispozicijom. Istočna mogućnost na SD-2 u jednokratnim blizancima dostiže 80% ili više. Većina pacijenata sa SD-2 ukazuje na prisustvo SD-2 za najbliže rođake; U prisustvu SD-2 u jednom od roditelja, verovatnoća njegovog potoka tokom života je 40%. Koji je jedan gen, čiji polimorfizam određuje predispoziciju za SD-2, nije otkrivena. Čimbenici okoliša igraju veliku važnost u sprovođenju nasljedne predispozicije za SD-2. Čimbenici rizika od rizika SD-2 su:
Gojaznost, posebno visceral (vidi odlomak 11.2);
Etnička pripadnost (posebno prilikom promjene tradicionalnog načina života na zapadnoj);
Sedentarni stil života;
Značajke prehrane (velika potrošnja rafiniranih ugljikohidrata i sadržaja niskog vlakana);
Arterijska hipertenzija.
Patogeneza
Patogenetski SD-2 je heterogena grupa metaboličkih poremećaja, upravo to utvrđuje njezinu značajnu kliničku heterogenost. Osnova njene patogeneze je otpornost na inzulinu (smanjenje posredovanog inzulina iskorištenosti glukoze tkiva), koji se provodi protiv pozadine sekretorne disfunkcije β-ćelija. Dakle, postoji kršenje ravnoteže osjetljivosti na sekreciju inzulina i inzulina. Tajni disfunkcijaβ - Flotato je usporiti "rano" sekretorni emisiju inzulina kao odgovor na porast glukoze u krvi. Istovremeno, prva (brza) faza izlučivanja, koja leži u pražnjoj vezi sa akumuliranim inzulinom, zapravo je odsutna; Druga (spora) faza izlučivanja vrši se kao odgovor na stabilizacijsku hiperglikemiju u toničnom režimu, a uprkos pretjeranom izlučivanju inzulina, nivo glikemije protiv pozadine otpornosti na inzulin nije normaliziran (Sl. 7.8).
Posljedica hiperinsulinemije je smanjiti osjetljivost i broj inzulinskih receptora, kao i suzbijanje
mehanizmi nakon receptora potiču uticaje inzulina (otpornost na inzulin).Sadržaj glavnog transportera glukoze u mišićnim i masnim ćelijama (Glut-4) smanjuje se za 40% kod osoba sa visceralnim pretilošću i 80% kod osoba sa SD-2. Zbog inzulinskog otpora hepatocita i portala hiperinsulinemije, hiperprodukcija glukoze, jetra,a hiperglikemija se razvija, koja se otkriva u većini pacijenata sa SD-2, uključujući u ranim fazama bolesti.
Sama hiperglikemija negativno utječe na prirodu i nivo sekretorne aktivnosti β-ćelija (glukotoksičnosti). Dugo, tokom godina i decenija, postojeća hiperglikemija na kraju dovodi do iscrpljenosti inzulinskih proizvoda β-ćelija, a neki simptomi mogu se pojaviti u pacijentu. nedostatak inzulina- mršavljenje, ketoza s pridruženim zaraznim bolestima. Međutim, preostali inzulinski proizvodi, koji su dovoljni za sprečavanje ketoacidoze, gotovo se uvijek sačuvano u SD-2.
Epidemiologija
SD-2 definira epidemiologiju SD-a u cjelini, jer čini oko 98% slučajeva ove bolesti. Prevalencija SD-2 varira u različitim zemljama i etničkim grupama. U evropskom
 Sl. 7.8.Tjektorica disfunkcije β-ćelija sa dijabetesom tipa 2 (gubitak prve faze eksplozije inzulina)
Sl. 7.8.Tjektorica disfunkcije β-ćelija sa dijabetesom tipa 2 (gubitak prve faze eksplozije inzulina)
zemlje, SAD i Ruska Federacija, to je oko 5-6% stanovništva. S godinama, učestalost SD-2 povećava se: među odraslima, prevalenca SD-2 iznosi 10%, među ljudima preko 65 doseže 20%. Incidencija SD-2 je 2,5 puta veća među autohtonim ljudima Amerike i Havajskih ostrva; Među Indijancima plemena Pima (Arizona) dostiže 50%. Među ruralnim stanovništvom Indije, Kine, Čile i afričke zemlje koje vode tradicionalni način života, rasprostranjenost SD-2 je vrlo mala (manja od 1%). S druge strane, među imigrantima u zapadnoj industrijskoj zemljama dostiže značajan nivo. Dakle, među imigrantima iz Indije i Kine koji žive u Sjedinjenim Državama i Velikoj Britaniji, prevalencija SD-2 dostiže 12-15%.
Ko predviđa povećanje broja bolesnika dijabetesa u svijetu za 122% u narednih 20 godina (sa 135 do 300 miliona). To je zbog progresivnog starenja stanovništva i distribucijom i pogoršanjem urbaniziranog načina života. Posljednjih godina došlo je do značajnog "podmlađivanja" SD-2 i rast njegove učestalosti među djecom.
Kliničke manifestacije
U većini slučajeva, izrečene kliničke manifestacije su odsutne,a dijagnoza je uspostavljena tokom rutinske definicije nivoa glikemije. Bolest se obično manifestuje starije od 40 godina, dok velika većina pacijenata ima pretilost i druge komponente metaboličkog sindroma (vidi stav 11.2). Pacijenti ne nameću žalbe na radni kapacitet ako nema drugih razloga za to. Žalbe žeđi i poliurije rijetko postižu značajnu ozbiljnost. Često su pacijenti zabrinuti za kožu i vaginalnu svrbež, a samim tim se okreću dermatolozima i ginekolozima. Od mnogih godina (u prosjeku oko 7 godina), mnogi pacijenti u vrijeme otkrivanja bolesti u kliničkoj slici, u vrijeme identifikacije bolesti u kliničkoj slici često su dominiraju iz stvarne manifestacije SD-2 prije dijagnoze. simptomi i manifestacije kasnih komplikacija SD-a.Štaviše, prva žalba pacijenta sa SD-2 za medicinsku pomoć vrlo je često zbog kasnih komplikacija. Dakle, pacijenti se mogu hospitalizovati u hirurškim bolnicama sa peptičnim lezijama nogu (dijabetični sindrom stopala),kontakt povezuje progresivnu viziju oftalmolozima (dijabetička retinopatija),hospitaliziran srčanim napadima, moždani udar
tami, kosi poraz broda u ustanovi, gdje prvo pronađu hiperglikemiju.
Dijagnostika
Dijagnostički kriteriji, uniforma za sve vrste SD-a predstavljeni su u klauzuli 7.3. Dijagnoza SD-2 u velikoj većini zasniva se na otkrivanju hiperglikemije u pojedincima sa tipičnim kliničkim znakovima SD-2 (gojaznost, starost više od 40-45 godina, pozitivnu porodičnu istoriju SD-2, ostale komponente metaboličkog sindroma ), u nedostatku kliničkih i laboratorijskih znakova apsolutni nedostatak inzulina (izraženi gubitak kilograma, ketoza). Kombinacija velike prevalencije SD-2, karakteristično za dugi asimptomatski protok i mogućnost sprečavanja njegovih teških komplikacija, podložnom ranoj dijagnozi, predodređene potrebe screeningoni. Ispitivanje kako bi se isključio SD-2 među pojedincima bez ikakvih simptoma bolesti. Glavni test, kako je naznačeno, je definicija nivo glikomije je prazan stomak.Prikazuje se u sljedećim situacijama:
1. Svi su ljudi stariji od 45 godina, posebno više od tjelesne težine (CMT više od 25 kg / m 2) u intervalima svake 3 godine.
2. U najmanjoj dobi u prisustvu viška tjelesne težine (BMI sa više od 25 kg / m 2) i dodatnih faktora rizika koji uključuju:
Sedentarni stil života;
SD-2 za najbliže rođake;
Koji pripada nacionalnom riziku razvoja SD-2 (Afroamerikanci, Latinoamerikanci, autohtoni Amerikanci itd.);
Žene koje su rodile djetetu vaganje više od 4 kg i / ili u prisustvu gestacijskog dijabetesa kao povijesti;
Arterijska hipertenzija (≥ 140/90 mm HG);
Nivo HDL\u003e 0,9 mmol / l i / ili trigliceridi\u003e 2,8 mmol / l;
Sindrom policističnog jajnika;
NTG i NGN;
Kardiovaskularne bolesti.
Značajno povećanje učestalosti SD-2 među djece diktira potrebu za definicijom skrininga nivoa glikemije među djecom i adolescentima(počevši od 10 godina s intervalom za 2 godine ili s početkom
pubertata, ako se pojavio u ranijoj dobi) koji pripada grupama povećanog rizika za koju djeca pripadaju sa obiljem tjelesne težine(BMI i / ili tjelesna težina\u003e 85 posto, odgovarajuće dobi ili težina veće od 120% u odnosu na idealnu) u kombinaciji sa bilo kojim dva navedena dodatnih faktora rizika:
SD-2 među rođacima prvog ili drugog reda srodstva;
Pripadajući nacionalnostima visokog rizika;
Kliničke manifestacije povezane sa otporom na inzulinu (Acantrosis Nigricans,arterijska hipertenzija, dislipidemija);
SD, uključujući gestacijsku, majku.
Diferencijalna dijagnoza
Diferencijalna dijagnoza SD-2 i SD-1, čiji su principi opisani u stavku 7.5 opisani su u stavku 7.5 (Tabela 7.6). Kao što je naznačeno, u većini slučajeva se temelji na podacima kliničke slike. U slučajevima kada uspostavljanje vrste CD-a ispunjava poteškoće, ili postoji sumnja na neka rijetka varijanta SD-a, uključujući u okviru nasljednih sindroma, najvažnije praktično pitanje na koje je potrebno odgovoriti je da li je pacijent Potreban vam je pacijent u terapiji inzulinom.
Tretman
Glavne komponente tretmana SD-2 su: dijetalna terapija, produženje fizičke aktivnosti, terapiju šećera, prevencija i liječenje komplikacija kasnih CD-a. Budući da većina pacijenata sa gojaznošću SD-2 trpi, dijeta treba biti usmjerena na smanjenu težinu (hipohalorial) i sprečavanje kasnih komplikacija, prije svega makroaganipatije (ateroskleroza). Hipolarska prehranapotrebno je za sve pacijente s viškom tjelesne težine (BMI 25-29 kg / m 2) ili pretilost (BMI\u003e 30 kg / m 2). U većini slučajeva treba preporučiti smanjiti dnevni rub hrane na 1000-1200 kcal za žene i do 1200-1600 kcal za muškarce. Preporučeni omjer glavne komponente hrane na SD-2 sličan je tome sa SD-1 (ugljikohidrati - 65%, proteini 10-35%, masti do 25-35%). Koristiti alkoholpotrebno je ograničiti zbog činjenice da je to suštinski izvor dodatnih kalorija, osim toga, prijem alkohola na pozadini Tere
sDI sa sulfonilurea i inzulinom mogu izazvati razvoj hipoglikemije (vidi stav 7.7.3).
Preporuke za proširenje fizičke aktivnostimora biti individualiziran. Na početku se preporučuje aerobična opterećenja (hodanje, plivanje) umjerenog intenziteta u trajanju od 30-45 minuta 3-5 puta dnevno (oko 150 minuta sedmično). Ubuduće je potrebno postepeno povećavati fizički napor, što značajno pomaže u smanjenju i normalizaciji tjelesne težine. Pored toga, fizički napor pomaže u smanjenju otpornosti na inzulinu i imati hipoglimiziranje učinka. Kombinacija dijetetherapije i proširenja fizičkog napora bez imenovanja lijekova za šećer omogućava održavanje SD kompenzacije u skladu s utvrđenim ciljevima (Tabela 7.3) otprilike 5% pacijenata sa SD-2.
Pripravci za Šetarska terapijakad se SD-2 može podijeliti u četiri glavne grupe.
I. Pripreme koji doprinose smanjenju otpornosti na inzulin (senzizeri).Ova grupa uključuje Metformin i Thiazolidiondije. Metforminje jedini koji trenutno koristi lijek iz grupe bivsuanids.Glavne komponente mehanizma njegove akcije su:
1. Suzbijanje glukonegeneze u jetri (smanjenje glukoznih proizvoda sa jetrom), što dovodi do smanjenja nivoa glikomije na prazan stomak.
2. Smanjenje otpornosti na inzulin (povećanje raspolaganja glukoze perifernim tkivima, prvenstveno mišićima).
3. Avnaeobično aktiviranje glikolize i smanjenje usisavanja glukoze u tamnom crevu.
Metforminpriprema je prvog izbora šećerne terapije kod pacijenata sa SD-2, gojaznošću i hiperglikemijom na prazan stomak. Početna doza je 500 mg po noćenju ili tokom večere. U budućnosti se doza postepeno povećava na 2-3 grama za 2-3 prijema. Među nuspojavama relativno često postoje dispeptičke pojave (proliv), koji, u pravilu, prolazni i prolaze samostalno nakon 1-2 tjedna od prijema lijeka. Budući da Metformin nema stimulativni učinak na inzulinske proizvode, na pozadini monoterapije od strane ove hipoglikemije lijekova
razviti (njegova akcija je označena kao antihiperglycemic, a ne kao hipoglikemic). Kontraindikacije na imenovanje metformina su trudnoća, teška srca, jetrena, bubrega i drugi neuspjeh organa, kao i hipoksična stanja druge geneze. Izuzetno rijetka komplikacija, koja se događa prilikom imenovanja Metformin bez uzimanja u obzir predstavljene kontraindikacije je laktacidoza, što je posljedica hiperaktivacije anaerobne glikolize.
Thiazolidindions(Pioglitazone, RosigtyaZon) su agonisti γ-receptora koji su aktivirali Peroxiz (PPAR-γ). Thiazolidindions aktiviraju metabolizam glukoze i lipida u mišićima i masnim tkivima, što dovodi do povećanja aktivnosti endogenog insulina, tj. Za uklanjanje otpornosti na inzulin (inzulinski senzizeri). Dnevna doza Pioglotazona je 15-30 mg / dan, Roseglitazone - 4-8 mg (na recepciji 1-2). Kombinacija tiazolidindiona sa metformom je vrlo efikasna. Kontraindikacija u svrhu tiazolidindija je povećanje (2,5 puta ili više) nivo jetrenih transaminaza. Pored hepatotoksičnosti, nuspojave tiazolidinskog EDION-a uključuju kašnjenje u tekućinu i oticanje, koji se češće razvijaju tokom kombinacije inzulinskih preparata.
II. Pripravci koji utiču naβ - Bolje i doprinose jačanju izlučivanja inzulina.Ova grupa uključuje sulfonske i glinene pripreme (prondijski glikemijski regulatori), koji se koriste uglavnom za normalizaciju nivoa glikemije nakon jela. Glavna meta pripravci sulfonylmohevina(PSM) su β-ćelije pankreatičkih ostrva. PSM veže se na β-ćelijsku membranu sa određenim receptorima. To dovodi do zatvaranja kalijuma ovisnih kalijevina ATP-a i depolarizacije ćelijske membrane, što zauzvrat doprinosi otvaranju kalcijum kanala. Protok kalcijuma unutar β-ćelije dovodi do njihove degranulacije i inzulinske emisije u krv. U kliničkoj praksi koristi se prilično puno PSMS-a, koji se razlikuju u trajanju i ozbiljnosti efekta šećera (Tabela 7.9).
Stol. 7.9.Pripravci sulfonylmohevina
 Glavna i prilično česta nuspojava PSM-a je hipoglikemija (vidi odlomak 7.7.3). Može se pojaviti sa predoziranjem droga, njenom kumulacijom (neuspjeh bubrega),
Glavna i prilično česta nuspojava PSM-a je hipoglikemija (vidi odlomak 7.7.3). Može se pojaviti sa predoziranjem droga, njenom kumulacijom (neuspjeh bubrega),
nepoštivanje dijeta (prolazno obroke, unos alkohola) ili režimu (značajan fizički napor, prije kojih doze PSM-a nije smanjena ili se ne uzimaju ugljikohidrati).
U grupu džinide(Prancijalni regulatori glikemije) repaglinid(derivat benzoične kiseline; dnevna doza 0,5-16 mg / dan) i nateglinida(D-fenililanski derivat; Dnevna doza od 180-540 mg / dan). Nakon uzimanja droga, priprema i reverzibilni sa sulfonylurevine receptorom na β ćeliji, kao rezultat toga, pojavi se kratko povećanje nivoa inzulina, što oponaša prva faza svoje lučenje normalno. Pripreme su prihvaćene za 10-20 minuta do glavnih obroka, obično 3 puta dnevno.
III. Pripravci koji smanjuju apsorpciju glukoze u crijevu.
Ova grupa uključuje Akaboz i guar smolu. Mehanizam djelovanja akarboze je reverzibilna blokada α-glikozidaze tankog crijeva, kao rezultat koji procesi uzastopnog fermentiranja i usisavanje ugljikohidrata usporavaju, brzina resorpcije i uvrštavanja glukoze u jetru smanjuje i Nivo postprandijske glikomije je smanjen. Početna doza akarboze je 50 mg 3 puta dnevno, u budućnosti se doza može povećati na 100 mg 3 puta dnevno; Lijek je prihvaćen neposredno prije jela ili za vrijeme hrane. Glavna nuspojava akarbose je crijevna dispepsija (dijareja, nadutost), koja je povezana sa primitkom ugljikohidrata koji nisu otkriveni u debelo crijev. Učinak sakrarizacije akarboze je vrlo umjeren (tablica 7.10).
U kliničkoj praksi, tablete sahachinching drogama se efikasno kombiniraju jedni s drugima i sa inzulinskim preparatima, jer se većina pacijenata istovremeno definira kao MercIlarnu i postprandičnu hiperglikemiju. Postoje brojni fiksne kombinacijepripreme u jednom tabletu. Najčešće u jednoj tabletu, metformin sa raznim PSMS-om, kao i metformin sa tiazolidiDinesiones, kombiniran je.
Stol. 7.10.Mehanizam djelovanja i potencijalne efikasnosti tabletih lijekova šećera
 IV. Inzulini i analogni insulina
IV. Inzulini i analogni insulina
U određenoj fazi, preparati inzulina počnu dobijati do 30-40% pacijenata sa SD-2. Indikacije za inzulinu terapiju u SD-2 predstavljene su početkom stava 7.4. Najčešća opcija za prijevod pacijenata sa SD-2 na inzulinskoj terapiji je dodijeliti inzulinu produžene akcije (inzulin NPH, Glargin ili Detech) u kombinaciji s primljenim tablistom lijekovima sa šećerom. U situaciji u kojoj nivo glikemije nije moguće kontrolirati imenovanje metformin ili posljednje kontraindicirano, pacijent je dodijeljen večernjim (noćenje) injekcijom inzulina. Ako je nemoguće kontrolirati uz pomoć tabletaičnih lijekova kao žive i postprandijske glikomije, pacijent je preveden u monoinzonaterapiju. Obično se sa tzvaznim terapijom SD-2 vrši na takozvanom "Tradicionalna" shema,što podrazumijeva imenovanje fiksnih doza inzulina produženih i kratkih radnji. U ovom planu
standardne mješavine inzulina koji sadrže kratku (ultrasort) i produženu radnju u jednoj boci su zgodni. Izbor tradicionalne terapije inzulinom određuje se činjenicom da je u SD-2, često imenovan za starije osobe čije je učenje nezavisnoj promjeni inzulinske doze teško. Pored toga, intenzivna inzulinska terapija, čija je svrha održavanja naknade za razmjenu ugljikohidrata na nivou koji se približava normatikemiji, povećava rizik od hipoglikemije. Ako za mlade pacijente, lagana hipoglikemija ne predstavlja ozbiljnu opasnost, kod starijih pacijenata sa smanjenim pragom osjetila hipoglikemije, mogu imati vrlo nepovoljne efekte iz kardiovaskularnog sistema. Mladi pacijenti sa SD-2, kao i pacijentima u pogledu efikasnih mogućnosti učenja, mogu se imenovati intenzivnom verzijom inzulinske terapije.
Prognoza
Glavni razlog invalidnosti i smrt pacijenata sa SD-2 su kasne komplikacije (vidi stavak 7.8), najčešće dijabetičke makroaganipatija. Rizik od razvoja određenih kasnih komplikacija određuje se kompleksom faktora koji se razgovaraju u relevantnim poglavljima. Univerzalni faktor rizika za njihov razvoj je hronična hiperglikemija. Dakle, smanjenje nivoa HbA1c kod pacijenata sa SD-2 na 1% dovodi do smanjenja ukupne smrtnosti za oko 20%, za 2% i 3% - za oko 40%, respektivno
7.7. Akutne komplikacije dijabetesa
7.7.1. Dijabetička ketoacidoza
Dijabetička ketoacidoza (dca)- Dekompenzacija SD-1, zbog apsolutnog nedostatka inzulina, u nedostatku pravovremenog liječenja završetka ketoacidotske kome (QC) i smrti.
Etiologija
Uzrok DCA je apsolutni nedostatak inzulina. To se ili ta ozbiljnost DCA određuje u većini pacijenata u trenutku manifestacije SD-1 (10-20% svih slučajeva DCA).
Pacijent s dijagnosticiranom dijagnozom DCA-e SD-1 može se razviti kada se inzulin zaustavi, često pacijent (13% slučajeva DCA), na pozadini istodobnih bolesti, prije svega zaraze, u nedostatku povećanja inzulina doza
Stol. 7.11.Dijabetička ketoacidoza
 Do 20% razvojnih slučajeva DC-1 u mladim pacijentima sa SD-1 povezani su sa psihološkim problemima i / ili poremećajima ponašanja hrane (strah od debljanja, strah od hipoglikemije, tinejdžerskih problema). Prilično česti uzrok dca u brojnim zemljama je
Do 20% razvojnih slučajeva DC-1 u mladim pacijentima sa SD-1 povezani su sa psihološkim problemima i / ili poremećajima ponašanja hrane (strah od debljanja, strah od hipoglikemije, tinejdžerskih problema). Prilično česti uzrok dca u brojnim zemljama je
odustani od inzulina od strane pacijenta zbog visokih troškova lijekova za neke sektore stanovništva (Tabela 7.11).
Patogeneza
U srcu patogeneze DCA nalazi se apsolutni nedostatak inzulina u kombinaciji s povećanjem proizvoda konjnurnih hormona, poput glukagona, kateholamina i kortizola. Kao rezultat toga, značajno je povećanje proizvoda glukozne jetre i poremećaja njegovog odlaganja perifernim tkivima, povećanjem hiperglikemije i poremećaja osmolarnosti vanćelijskog prostora. Manjak inzulina u kombinaciji s relativnim viškom o hormonima na DCA-u dovodi do oslobađanja besplatnih masnih kiselina (lipoliza) i njihove nekomprimirane oksidacije u jetri do ketonske tijela (β-hidroksibutirat, acetone, kao rezultat čije hipercohememije razvija i u budućoj metaboličkoj acidozi. Kao rezultat izražene glukoze, osmotski diuresis razvija se, dehidracija, gubitak natrijuma, kalijum i druge elektrolite (Sl. 7.9).
Epidemiologija
Učestalost novih slučajeva DCA iznosi 5-8 na 1000 pacijenata sa SD-1 godišnje i direktno ovisi o nivou organizacije medicinske pacijente sa SD-om. Svake godine u Sjedinjenim Državama javlja se oko 100.000 hospitalizacija o DCA, dok uzimajući u obzir troškove jednog pacijenta za hospitalizaciju od 13 hiljada dolara, više od milijardu dolara godišnje utrošeno je na stacionarno liječenje DCA-e. U Ruskoj Federaciji u 2005. godini DKA je zabilježen u 4,31% djece, 4,75% adolescenata i 0,33% odraslih pacijenata sa SD-1.
Kliničke manifestacije
Ovisno o uzroku uzroka, ovisno o uzroku uzrokovanom razlogom, može potrajati od nekoliko tjedana u dan. U većini slučajeva DCA prethodi dijabetes dekompenzacija simptoma, ali ponekad možda nemaju vremena za razvoj. Klinički simptomi DCA uključuju poliuria, polidipsiju, mršavljenje, proliveni trbušni bolovi ("dijabetični pseudoperitonite"), dehidracija, izražena slabost, miris acetona iz usta (ili voćnog mirisa), postepeno zamagljujući svijest. Prava koma na DCA nedavno se razvija relativno rijetko zbog rane dijagnoze. U fizičkim istraživanjima otkrivaju se znakovi dehidracije: smanjenje
 Sl. 7.9. Patogeneza ketoacidotske kome
Sl. 7.9. Patogeneza ketoacidotske kome
turgor kože i gustoće očnih jabučica, tahikardija, hipotenzija. U slučajevima u nastajanju razvija se disanje Kussmoula. Više od 25% pacijenata s DCA razvija povraćanje, što može ličiti na kavu debljinu boje.
Dijagnostika
Zasnovan je na kliničkim podacima o slici, naznake prisutnosti pacijenta SD-1, kao i podacima laboratorijske studije. Za DCA je karakterizirana hiperglikemija (u nekim slučajevima, beznačajnom), ketonurijom, metaboličkom acidozom, hiperosistolarnošću (tablica 7.12).
Stol. 7.12.Laboratorijska dijagnostika oštrih komplikacija dijabetesa
 Prilikom ispitivanja pacijenata s akutnom dekompenzacijom SD-a potrebno je odrediti nivo glikemije, kreatinina i uree, elektrolita na osnovu koje se izračunava efikasna osmolarnost. Pored toga, potreban je pratnja i zemlja. Efikasna osmolarnost(EO) se izračunava prema sljedećoj formuli: 2 *. Norma EO je 285 - 295 mosm / l.
Prilikom ispitivanja pacijenata s akutnom dekompenzacijom SD-a potrebno je odrediti nivo glikemije, kreatinina i uree, elektrolita na osnovu koje se izračunava efikasna osmolarnost. Pored toga, potreban je pratnja i zemlja. Efikasna osmolarnost(EO) se izračunava prema sljedećoj formuli: 2 *. Norma EO je 285 - 295 mosm / l.
Određuje se većina pacijenata sa DCA leukocitozaŠto je ozbiljnost proporcionalnog nivou ketonskog tijela u krvi. Razina natrijumu pravilu se smanjuje zbog osmotskih izliva tekućine iz unutarćelijskih prostora do izvanselularne kao odgovor na hiperglikemiju. Manje često natrijum-nivo može se lažno smanjiti kao rezultat izraženog hiper-
trigliceridemija. Razina kalijumserum se može u početku povisiti zbog svog pokreta iz vanselularnih prostora.
Diferencijalna dijagnoza
Ostali razlozi za gubitak svijesti kod pacijenata sa SD-om. Diferencijalna dijagnoza sa hiperosmolarnom kome, u pravilu ne uzrokuje poteškoće (razvija se u starijim pacijentima sa SD-2) i nema veliku kliničku vrijednost, jer Principi liječenja obje države su slični. Ako je nemoguće brzo otkriti razlog gubitka pacijentove svijesti s SD-om, prikazuje se uvođenje glukoze, od tada Hipoglikemijske države se nalaze mnogo češće, a brza pozitivna dinamika protiv pozadine uvođenja samog glukoze omogućava nam da otkrijemo razlog gubitka svijesti.
Tretman
Liječenje DKA-a podrazumijeva rehidraciju, korekciju hiperglikemije, poremećaja elektrolita, kao i liječenje bolesti koje su prouzrokovale dekompenzacija dijabetesa. Tretman je najoptimalniji u odjelu za oživljavanje specijalizirane medicinske ustanove. Kod odraslih pacijenata bez strogo istodobne srčane patologije, još uvijek u prednceratnoj fazi kao primarnu mjeru za svrhu reydratumentpreporučuje se uvođenje izotoničnog rješenja (0,9% nacl) otprilike brzinom litre na sat (oko 15-20 ml po kilogramu težine na sat). Potpuna nadoknada nedostatka tekućine, koji je sa DCA-om 100-200 ml po kg kilograma, mora se postići u prvim danima liječenja. S istodobnim zatajenjem srca ili bubrega, ovaj vremenski period mora biti povećan. Za djecu, preporučeni volumen izotoničkog rješenja za terapiju rehidražama iznosi 10-20 ml po kg tjelesne težine na sat, a u prvih 4 sata ne smije prelaziti 50 ml po kg kilograma. Preporučuje se puna rehidratacija za postizanje otprilike 48 sati. Nakon u pozadini paralelne terapije inzulina, nivo glikemije će se smanjiti oko 14 mmol / l, ići na transfuziju 10% rješenja glukoze, što nastavlja s rehidracijom.
Trenutno usvojen koncept "malih doza" insulinu tretmanu dca. Koristi se samo kratki akcija inzulina. Najoptimalnije korištenje intravenske institutke
lina. Intramuskularno uvođenje inzulina, što je manje efikasno, moguće samo s umjerenom težinom DCA, sa stabilnom hemodinamikom i ako je nemoguće za intravensku terapiju. U drugom slučaju, injekcije se izrađuju u ravnom mišiću trbuha, dok se igla za intramuskularne injekte postavlja na inzulin špric (za pouzdan intramuskularni hit), a na ovoj iglici se inzulin regrutuje iz boce u špricu u špricu .
Postoji nekoliko opcija za intravensku administraciju inzulina. Prvo, inzulin se može uvesti "u gumeni pojas" infuzijskog sistema, dok se potrebna količina inzulina bude stečena u inzulinsku špricu, nakon čega se dobija 1 ml izotoničkog rješenja. Do dostizanja nivoa glikomije, 14 mmol / l je sat sa po satu uveden 6-10 jedinica kratke akcije; dalje (Paralelno s promjenom rehidracijskog rješenja sa izotonikom za 10% glukoze)ovisno o vremenu definiranih pokazatelja glikemije, doza inzulina smanjuje se na 4-8 jedinica na sat. Preporučena stopa smanjenja nivoa glikemije ne bi trebala prelaziti 5 mmol / l na sat. Druga utjelovljenje intravenske terapije inzulina podrazumijeva upotrebu perfuzora. Za pripremu produženika, 2 ml 20% otopine ljudskog albumina dodaje se na 50 mg izotoničkog rješenja od 0,9%. Ako je odabrana intramuskularna puta inzulinske administracije, u početku se u početku uvedena 20 jedinica kratke akcije, nakon čega je 6 jedinica, a nakon postizanja nivoa glikemije 14 mmol / l doseže se na 4 jedinice na sat. Nakon potpune stabilizacije hemodinamike i naknade za poremećaje kiseline, pacijent je preveden u subkutane injekcije inzulina.
Kao što je naznačeno, uprkos značajnim nedostatak kalijumau tijelu (ukupni gubitak od 3-6 mmola / kg), s DCA-om je njegov nivo prije početka inzulinske terapije može biti donekle povišen. Ipak, početak transfuzije rješenja kalij hlorida preporučuje se istovremeno s početkom inzulinske terapije, ako je nivo kalijuma plazme manji od 5,5 mmol / l. Uspješna korekcija nedostatka kalijuma događa se samo na pozadini pH normalizacije. Sa niskim pH unos kalijuma znatno se smanjuje, u vezi s tim, ako je moguće, doziranje prelijevanja kalijum-hlorida poželjno se prilagoditi određenom pH indikatoru (tablica 7.13).
Stol. 7.13.Shema korekcije kalijskog deficita
 * Za izračun, sledeći podaci koriste:
* Za izračun, sledeći podaci koriste:
1 g kcl \u003d 13.4 mmol; 1 mmol kcl \u003d 0,075 g. U roku od 4% KS1: u 100 ml - 4 g KS1, u 25 ml - 1 g KS1, u 10 ml od 0,4 g KS1.
Razlog za dekompenzacija dijabetesa često je zarazne bolesti(Pyelonefritis, zaraženi čir s sindromom noga dijabetičara, upala pluća, sinusitisa i tako dalje.). Postoji pravilo u skladu s kojom se sa DCA antibiotikom terapija propisuje gotovo svim pacijentima sa podferilitacijom ili groznicom, čak i u nedostatku vidljivog fokusa infekcije, jer zapravo za zapravo za DCA, povećanje tjelesne temperature nije tipično.
Prognoza
DCA smrtnost je 0,5-5%, dok je većina slučajeva zbog kasne i nekvalificirane medicinske njege. Smrtnost je najveća (do 50%) među starijim pacijentima.
7.7.2. Hiperosmolarna koma
Hiperosmolarna koma(Gok) - rijetka akutna komplikacija SD-2, razvijajući se zbog izražene dehidracije i hiperglikemije protiv odsustva apsolutnog nedostatka inzulina, praćen visokom smrtnošću (Tabela 7.14).
Etiologija
Gok, u pravilu se razvija u starijim pacijentima sa SD-2. Takvi pacijenti najčešće su usamljeni, žive bez brige, zanemareni njihovim stanjem i samokontrolom i nemaju dovoljno tekućine. Često infekcija (sindrom dijabetičkog stopala, pneumonija, akutna pijalonefritis), poremećaji mozga vode do dekoppanzije
cirkulatorni i drugi uvjeti, kao rezultat kojih se pacijenti loše kreću, ne uzimajte drogu na bazi šećera i tečnost.
Stol. 7.14.HyroSmolarna koma (gok)
 Patogeneza
Patogeneza
Povećana hiperglikemija i osmotski diureza određuju izraženu dehidraciju, što je iz gore navedenih razloga ne ispunjeno izvana. Rezultat hiperglikemije i dehidracije je hiperosmoobelarnost plazme. Integralna komponenta patogeneze GOK-a je relativni nedostatak inzulina i višak protupolnih hormona, koji nastaju u SD-2, preostala sekrecija Insulina dovoljna je za suzbijanje lipolijase i ketogeneze, kao rezultat od kojih se ketoacidoza ne događa.
U nekim slučajevima, umjerena indukcija acidoze može se odrediti kao rezultat hipertaktatemije protiv pozadine hipoperfuzije tkiva. Sa izraženom hiperglikemijom za očuvanje osmotske ravnoteže u cerebrospinalnoj tekućini, natrijum-sadržaj koji dolazi iz ćelija mozga povećava gdje kalijum dođe u zamjenu. Počasnost od prijemnogbrana nervozne ćelije je poremećen. Progresivna perizam svijesti u kombinaciji sa konvulzivnim sindromom se razvija (Sl. 7.10).
Epidemiologija
Gok čini 10-30% akutnih hiperglikemijskih država u odraslima i starijim pacijentima sa SD-2. Otprilike 2/3 slučajeva Goka razvija se u osobama s nedijagnosticiranim u ovom Dia.
Kliničke manifestacije
Značajke kliničke slike hiperoslorosporedne kome su:
Kompleks znakova i komplikacija dehidracije i hipoperfuzije: žeđ, suvoća sluznih membrana, tahikardija, arterijske hipotenzije, mučnine, slabost, šok;
Fokusne i generalizirane konvulzije;
Groznica, mučnina i povraćanje (40-65% slučajeva);
Od istodobnih bolesti i komplikacija, točno se nalazi tromboza dubokih vena, pneumonija, poremećaji mozga, gastropareza.
Dijagnostika
Zasnovan je na podacima kliničke slike, dob pacijenta i istoriji SD-2, izrečene hiperglikemijom u odsustvu Ketonurije i ketoacidoze. Tipični laboratorijski znakovi Goka predstavljeni su u tabeli. 7.12.
 Sl. 7. .10.
Patogeneza hiperoslorosporedne kome
Sl. 7. .10.
Patogeneza hiperoslorosporedne kome
Diferencijalna dijagnoza
Ostale akutne države koje se razvijaju kod pacijenata sa dijabetesom, najčešće sa istodobnom patologijom koja vodi do izražene dekompenzacije SD-a.
Tretman
Liječenje i praćenje u GOK-u, osim nekih značajki, ne razlikuju se od onih opisanih za Ketoacidotsko dijabetičku komu (klauzulu 7.7.1):
Veća količina početne rehidracije od 1,5-2 litara po 1. času; 1 L - za 2. i 3. sat, zatim 500 ml / h izotonično otopino natrijum-hlorida;
Potreba za uvođenjem rješenja koja sadrže kalijum obično je veća od ketoacidotske kome;
Inzulinska terapija slična je onoj sa CC-om, ali potreba za inzulinom je manja, a nivo glikemije mora biti smanjen brže od 5 mmol / l na sat kako bi se izbjegao razvoj edema mozga;
Uvođenje hipotoničnog rješenja (NACL 0,45%) bolje je izbjeći (samo s izraženom hipernemijom:\u003e 155 mmol / l i / ili efikasna osmolarite\u003e 320 MO / L);
U uvođenju bikarbonata nema potrebe (samo u specijalizovanim režiserskim pretincima sa acidozom sa pH< 7,1).
Prognoza
Smrtnost na GOK-u je visoka i iznosi 15-60%. Najgora prognoza kod starijih pacijenata sa ozbiljno pratećom patologijom, koja je često uzrok dekompenzacije SD-a i razvoja Goka.
7.7.3. Hipoglikemija
Hipoglikemija- smanjenje nivoa glukoze u krvnom serumu (<2,2- 2,8 ммоль/л), сопровождающее клинический синдром, характеризующийся признаками активации симпатической нервной системы и/или дисфункцией центральной нервной системы. Гипогликемия как лабораторный феномен не тождественен понятию «гипогликемическая симптоматика», поскольку лабораторные данные и клиническая картина не всегда совпадают.
Etiologija
Predoziranje predoziranja inzulinskih preparata i njegovih analoga, kao i sulfonilurea lijekova;
Nedostatak hrane na pozadini nepromijenjene terapije šećerom;
Prihvatanje alkoholnih pića;
Fizički napor na pozadini nepromijenjene terapije šećerom i / ili bez dodatnog prijema ugljikohidrata;
Razvoj kasnih komplikacija SD-a (autonomna neuropatija sa gastroparezom, bubrežnim zatajenjem) i brojne druge bolesti (nadbubreni neuredni, hipotireoidizam, zatajenje jetre, maligni tumori) sa nepromijenjenim terapijom šećerom (nastavak recepcije i kumulacije TSP-a na pozadini bubrežnog zatajenja, očuvanje bivšeg doze inzulina);
Kršenje insulinske uprave (intramuskularno ubrizgavanje umjesto potkožnog);
Umjetna hipoglikemija (svjesna predoziranje lijekova šećera od strane pacijenta);
Organski hiperinulinizam - inzulin (vidi odlomak 10.3).
Patogeneza
Patogeneza hipoglikemije je da krši ravnotežu između protoka glukoze u krv, njegova zbrinjavanje, nivo inzulina i konjunurnih hormona. Obično, na nivou glikemije, u roku od 4,2-4,7 mmol / l, proizvodi i puštanje inzulina iz β-ćelija su potiskuju. Smanjenje nivoa glikomije manje od 3,9 mmol / l prati stimulaciju konjunralnih hormonskih proizvoda (glukagon, kortizol, hormon rasta, adrenalinom). Neuroglikopeni se simptomi razvijaju sa smanjenjem nivoa glikomije manji od 2,5-2,8 mmol / l. Za predoziranje insulini / ili droge sulfonylmochinahipoglikemija se razvija zbog direktnog hipoglimiziranog učinka egzogenog ili endogenog hormona. U slučaju predoziranja pripremama sulfonylurea, hipoglikemijski simptomi mogu se više puta ponoviti nakon obvezanja napada zbog činjenice da trajanje niza lijekova može doći do dana ili više. TSP, koji nemaju stimulativni učinak na inzulinske proizvode (metformin, tiazolidindions), sami hipoglikemiju ne mogu biti uzrokovane sami, ali kada dodaju sulfonylurea ili inzulin, prijem potonjeg u istoj dozi može uzrokovati hipoglikemiju zbog Kumulacija Shah-navigacijskog efekta kombinirane terapije (tablica. 7.15).
Stol. 7.15.Hipoglikemija
 Krajnja tablica. 7.15
Krajnja tablica. 7.15
 Prilikom primanja alkoholjavlja se suzbijanje glukegeneze u jetri, što je najvažniji faktor koji se suprotstavljaju hipoglikemiji. Fizička vježbazaštitite iskorištenost glukoze ovisne o inzulinu, zbog kojih se nalaze uzroci hipoglikemije na pozadini nepromijenjene terapije šećera i / ili u nedostatku dodatnog prijema ugljikohidrata.
Prilikom primanja alkoholjavlja se suzbijanje glukegeneze u jetri, što je najvažniji faktor koji se suprotstavljaju hipoglikemiji. Fizička vježbazaštitite iskorištenost glukoze ovisne o inzulinu, zbog kojih se nalaze uzroci hipoglikemije na pozadini nepromijenjene terapije šećera i / ili u nedostatku dodatnog prijema ugljikohidrata.
Epidemiologija
Svjetlo, brzo mjehuriće hipoglikemije kod pacijenata sa SD-1, primajući intenzivnu inzulinu terapiju, može se razviti nekoliko puta sedmično, a relativno bezopasna. Po pacijentu koji je na intenzivnoj inzulin terapiji, na čemu se navodi za 1 slučaj teške hipoglikemije. U većini slučajeva hipoglikemija se razvija noću. Sa SD-2 u 20% pacijenata koji primaju inzulin, a u 6% primaju sulfonske pripreme, za barem jednu epizodu teške hipoglikemije razvija se za barem jednu epizodu.
Kliničke manifestacije
Razdvajaju se dvije glavne grupe simptoma: adrenergički, povezani s aktiviranjem simpatičkog nervnog sustava i emisije adrenalinskih adrenalina i neuroglikopenika, povezane s oštećenim funkcioniranjem centralnog nervnog sistema protiv pozadine deficita svoje glavne energetske supstrate. Do adrenergičkisimptomi uključuju: tahikardiju, midriasis; anksioznost, agresivnost; Driver, hladan znoj, parestezija; Mučnina, snažna glad, hipersalizacija; Proliv, obilno mokrenje. Do neuroglikopeničansimptomi uključuju asteniju,
smanjenje koncentracije pažnje, glavobolje, osjećaj straha, zbrke, dezorijentacije, halucinacije; Govorni, vizualni, bihevioralni poremećaji, amnezija, kršenje svijesti, konvulzije, prolazne paralize, kome. Jasna ovisnost ozbiljnosti i niza razvoja simptoma kao hipoglikemiju možda neće biti. Mogu se pojaviti samo adrenergički ili samo neuroglikopeni simptomi. U nekim slučajevima, uprkos restauraciji normoglikokemije i stalne terapije, pacijenti mogu biti u kliznom ili ravnomjernoj stazi za komatoze tokom nekoliko sati, pa čak i dana. Dugoročna hipoglikemija ili njegove česte epizode mogu dovesti do nepovratnih promjena u centralnom nervnom sustavu (prvenstveno u kortezu velikih hemisfera), čija su manifestacije značajno razlikuju od ukusnih i halucinatorskih paranoidnih epizoda do tipičnih epileptičnih napada, što je neizbježni ishod od kojih su otporna demencija.
Hiperglikemija je subjektivno prebačena na pacijente lakšim od epizoda čak i lagane hipoglikemije. Stoga mnogi pacijenti zbog straha od hipoglikemije smatraju da je potrebno održavati glikemiju na relativno visokom nivou, što zapravo odgovara dekomentiranju bolesti. Prevladavanje ovog stereotipa zahtijeva znatne napore ljekara i obuke osoblja.
Dijagnostika
Klinička slika hipoglikemije u pacijentu sa SD-om u kombinaciji sa laboratorijom (u pravilu, s mjeračem glukoze) otkrivajući nizak nivo glukoze u krvi.
Diferencijalna dijagnoza
Ostali razlozi koji vode do gubitka svijesti. Ako je uzrok gubitka svijesti pacijenta SD-a nepoznat i nemoguće je provoditi ekspresnu analizu nivoa glikemije, pokazuje uvođenje glukoze. Često postoji potreba da saznate uzroke razvoja česte hipoglikemije kod pacijenata sa SD-om. Najčešće su posljedica neadekvatne terapije sa šećerom i znanje pacijenta niske razine o njihovoj bolesti. Treba imati na umu da bi se smanjila potreba za terapijom šećerom do potpunog otkazivanja ("nestali SD") može dovesti niz bolesti (nadbubrežna insuficijencija, hipotiroidizam, bubrežnog i jetre), uključujući zloćudne tumore.
Tretman
Za liječenje svjetlosnog hipoglikemije u kojem je pacijent svjestan i može se pomoći sebi, obično je dovoljno uzimati hranu ili tekućinu koja sadrži ugljikohidrate u iznosu od 1-2 kruha (10-20 g glukoze). Takav broj sadrži, na primjer, u 200 ml slatkog voćnog soka. Piće učinkovito zaustavlja hipoglikemiju, jer u tečnoj formi znatno se apsorbira glukoza. Ako simptomi i dalje rastu, uprkos kontinuiranom prijemu ugljikohidrata, potrebno je intravensko primjena glukoze ili intramuskularnog glukagona. Na isti način se teška hipoglikemija tretira sa gubitkom svijesti. U ovom slučaju pacijent je uveden oko 50 ml 40% rješenje glukoze intravenski.Uvođenje glukoze mora se nastaviti sve do obvezanja napada i normalizacije glikemije, iako je više doza do 100 ml i više, u pravilu nije potrebno. Glucagonuvodi se (u pravilu pripremljeno u tvorničkim uvjetima ispunjenim špric) intramuskularno ili supkutano. Nakon nekoliko minuta normalizira se nivo glikemije zbog indukcije glukoenolize glukagen. Međutim, to se ne događa uvijek: sa visokim nivoom inzulina u glukagonu u krvi neefikasan je. Polu-život glukagona kraći je od inzulina. Sa alkoholizmom i jetrom, sinteza glikogena je uznemirena, a administracija glukagona može biti neefikasna. Povratna efekat glukagove mogu se povraćati koja stvara opasnost od težnje. Zatvorite pacijent po mogućnosti vlastite tehnike ubrizgavanja glukagone.
Prognoza
Lagana hipoglikemija u obučenim pacijentima protiv pozadine dobre kompenzacije bolesti je sigurna. Česta hipoglikemija znak su lošeg kompenzacije SD-a; U većini slučajeva takvi pacijentima tokom ostatka dana određeni su više ili više izražene hiperglikemije i visok nivo glictenog hemoglobina. Stariji pacijenti sa kasnim komplikacijama hipoglikemije SD-a mogu izazvati takve vaskularne komplikacije kao infarkt miokarda, moždani udar, mrežni krvarenje. Hipoglikemijska koma traje do 30 minuta sa odgovarajućim tretmanom i brzom povratkom svijesti, u pravilu nema komplikacije i posljedice.
7.8. Kasne komplikacije dijabetesa
Kasne komplikacije se razvijaju s obje vrste SD-a. Klinički raspoređuju pet glavnih kasnih komplikacija SD: makroaganipatija, nefropatije, retinopatiju, neuropatije i dijabetičke nožnog sindroma. Nepouzdanost kasnih komplikacija za pojedine vrste SD određuje se činjenicom da je njihova glavna patogenetska veza hronična hiperglikemija. S tim u vezi, u vrijeme manifestacije SD-1, kasne komplikacije kod pacijenata gotovo se nikada ne susreću, razvijaju se kroz godine i decenijama, ovisno o efikasnosti terapije. Najveća klinička vrijednost u SD-1, u pravilu, stica dijabetička mikroaganipatipa(neuropatija, retinopatija) i neuropatija (dijabetički sindrom stopala). Sa SD-2, naprotiv, kasne komplikacije su često otkrivene u trenutku dijagnoze. Prvo, to je zbog činjenice da se SD-2 manifestira mnogo prije nego što se dijagnoza utvrdi. Drugo, ateroskleroza, klinički manifestuju makroaganipatipati, ima puno patogeneze uobičajene sa SD-om. Sa SD-2, najveći klinički značaj, u pravilu, stječe dijabetičare macroaganiopatija,Što se u vrijeme dijagnoze otkrije iz ogromne većine pacijenata. U svakom konkretnom slučaju, skup i ozbiljnost pojedinih kasnih komplikacija razlikuju se od njihovog paradoksalnog potpunog odsustva, uprkos značajnom trajanju bolesti do kombinacije svih mogućih opcija u teškom obliku.
Kasne komplikacije su glavni uzrok smrtipacijenti sa SD-om i uzimajući u obzir njegovu prevalenciju - najvažniji medicinski i socijalni problem zdravstvene zaštite većine zemalja. U vezi glavna svrha liječenjaa zapažanja pacijenata sa CD-om su prevencija (primarna, srednja, tercijarna) njegovih kasnih komplikacija.
7.8.1. Dijabetička makroaganipatipati
Dijabetička makroaganipatipati- kolektivni koncept koji kombinira aterosklerotsku leziju velikih arterija u SD-u,
klinički se očituje ishemijskom srčanom bolešću (IBS), kosi ateroskleroza mozga, donjih ekstremiteta, unutrašnjih organa i arterijske hipertenzije (tablica 7.16).
Stol. 7.16.Dijabetička makroaganipatipati
 Etiologija i patogeneza
Etiologija i patogeneza
Vjerovatno sličan etiologiji i patogenezi ateroskleroze kod pojedinaca bez SD-a. Aterosklerotski plakovi ne razlikuju se u mikroskopskoj strukturi u pojedincima s SD-a i bez njega. Ipak, sa SD-om u prvom planu mogu se izvesti dodatni faktori rizika, ili SD pogoršati dobro poznate nesedljive faktore. Kao takav, SD treba sadržavati:
1. Hiperglikemija.To je faktor rizika za aterosklerozu. Povećanje nivoa HbA1c za 1% kod pacijenata sa SD-2 Povećanjem
rizik od razvoja infarkta miokarda za 15%. Atherogeni akcijski mehanizam hiperglikemije nije sasvim jasan, moguće je da je povezan sa glikozacijom konačnih proizvoda metabolizma LDL-a i kolagena vaskularnog zida.
2. Arterijska hipertenzija(AG). U patogenezi su veliku važnost pričvršćena na komponentu bubrega (dijabetička nefropatija).AG sa SD-2 - ne manje značajan infarkt i faktor rizika od moždanog udara od hiperglikemije.
3. Dislipidemija.Hiperinstrulamija, koja je neotuđivana komponenta otpornosti na inzulin u SD-2, uzrokuje smanjenje nivoa HDL-a, povećavajući nivo triglicerida i smanjenje gustoće, I.E. Jačanje aterogenog LDL-a.
4. Gojaznost,sa kojim većinom pacijenata sa SD-2 pati, je neovisna faktor rizika ateroskleroza, infarkt miokarda i moždani udar (vidi odlomak 11.2).
5. Izulin otpor.Hiperinsulamija i visoki nivoi molekula nalik na inzulin-proinsulin povećavaju rizik od ateroskleroze koja može biti povezana s endotelnom disfunkcijom.
6. Poremećaj koagulacije krvi.Na SD-u, povećanje nivoa fibrinogena, aktivator inhibitora trombocita i Willebrand faktora, kao rezultat čije se formira protrombotsko stanje koaguliranog krvnog sustava.
7. Endotelna disfunkcija,karakterizirano povećanjem izražavanja aktivatora inhibitora plazminatora i molekula za adheziju ćelija.
8. Oksidativni stresšto dovodi do povećanja koncentracije oksidiranog LDL i F2-ISO-Perts.
9. Sistemska upalau kojem se povećava izraz fibrinogena i c-reaktivnog proteina.
Najznačajniji faktori za rizik od razvoja IWC-a na SD-2 su povišeni nivo LDL, smanjene HDL, arterijske hipertenzije, hiperglikemije i pušenja. Jedna od razlika aterosklerotskog procesa na SD-u češća je i distalna priroda okluzalne lezije,oni. Proces je češće uključen u relativno manje arterije, što otežava hirurško liječenje i pogoršava prognozu.
Epidemiologija
Rizik od razvoja IBS-a u osobama sa SD-2 6 puta veći od onih bez dijabetesa, dok je isti za muškarce i žene. Arterijska hipertenzija otkriva se u 20% pacijenata sa SD-1 i 75% iz SD-2. Općenito, kod pacijenata sa SD-om, susreće se 2 puta češće od onih bez njega. Orkupska ateroskleroza perifernih posuda razvija se u 10% pacijenata sa SD-om. Thromboembolizam moždanih žila razvija se u 8% pacijenata sa SD-om (2-4 puta češće od onih bez SD).
Kliničke manifestacije
Uglavnom se ne razlikuju od onih onih bez SD-a. U kliničkoj slici makrovaskularnih komplikacija SD-2 (infarkt miokarda, moždanog udara, okluzivne štete na pločicama stopala) često igraju prednji, a upravo je prvi put po prvi put hiperglikemija u njihovom razvoju u pacijentu. Možda zbog pratećeg autonomne neuropatije do 30% infarkta miokarda u osobama sa CDS-om, bez tipičnog angiosky napada (infarkt biroa).
Dijagnostika
Principi dijagnoze komplikacija ateroskleroze (IBS, oštećenje mozga, okluzivno oštećenje arterija nogu) ne razlikuju se od onih za pojedince bez SD-a. Mjera arterijski pritisak(Oglas) treba izvesti u svakoj posjeti pacijentu s SD ljekarom, a definicija pokazatelja lipidni spektarkrv (ukupni holesterol, trigliceridi, LDL, HDL) na SD-u mora se izvesti najmanje jednom godišnje.
Diferencijalna dijagnoza
Ostale kardiovaskularne bolesti, simptomatska arterijska hipertenzija, sekundarna dlipidemija.
Tretman
♦ Kontrola krvnog pritiska.Pravilan nivo sistolnog krvnog pritiska na SD-u je manji od 130 mmHg, a dijastolički 80 mmng (Tabela 7.3). Većina pacijenata treba nekoliko hipotenzivnih lijekova za postizanje ovog cilja. Lijekovi za izbor hipotenzivne terapije na CD-u su inhibitori ACE i blokatori receptora angiotenzin, koji, ako je potrebno, nadopunjuju tiazidni diuretici. Pripravci za odabir za pacijente sa SDS-om koji su podvrgnuti miokardnom infarktu su β-adrenoblays.
♦ Ispravljanje odlipidemije.Ciljni nivoi pokazatelja lipidnih spektra prikazani su u tablici. 7.3. Pripreme izbora hipolipidemijske terapije su inhibitori 3-hidroksi-3-metilglu-ko-reduktaze (statini).
♦ Antiagregantna terapija.Terapija aspirina (75-100 mg / dan) prikazana je pacijentima sa SD starijem od 40 godina s povećanim rizikom razvoja kardiovaskularne patologije (opterećena porodična povijest, arterijska hipertenzija, pušenje, kao i svim pacijentima) sa kliničkim manifestacijama ateroskleroze kao sekundarnih profilaksa.
♦ Projekcija i liječenje IBS-a.Testovi opterećenja za isključenje IBS-a prikazani su pacijentima sa simptomima kardiovaskularnih bolesti, kao i prilikom identifikacije patologije u EKG-u.
Prognoza
75% pacijenata sa SD-2 i 35% pacijenata sa SD-1 umire od kardiovaskularnih bolesti. Otprilike 50% pacijenata sa SD-2 umire od komplikacija CHD, 15% mozga plovila Thromboemboliam. Smrtnost od infarkta miokarda kod osoba sa SD-om prelazi 50%.
7.8.2. Dijabetička retinopatija
Dijabetička retinopatija(Dr) - mikroaktipatija mrežnih žila oka, karakterizirana razvojem mikroenvirnment, krvarenja, eksudativnih promjena i širenja novoformiranih plovila, što dovodi do djelomičnog ili potpunog gubitka vizije (Tabela 7.17).
Etiologija
Glavni etiološki faktor u razvoju dr je hronična hiperglikemija. Ostali faktori (arterijska hipertenzija, dislipidemija, pušenje, trudnoća itd.) Imaju manje važnosti.
Patogeneza
Glavne veze patogeneze DR su:
Mrežna plovila Microaganiopatipatija, koja vodi do suženju nadzora plovila sa razvojem hipoperfuzije;
Degeneracija plovila sa formiranjem mikronevnosti;
Progresivna hipoksija, stimulativna širenja plovila i vodeći do masne distrofije i taloženje kalcijum soli u mrežnice;
Stol. 7.17.Dijabetička retinopatija
 Mikroindarrcts s \u200b\u200bekspodracijom, što dovodi do stvaranja mekih "pamučnih tačaka";
Mikroindarrcts s \u200b\u200bekspodracijom, što dovodi do stvaranja mekih "pamučnih tačaka";
Taloženje lipida sa formiranjem gustih eksudata;
Rast mrežnice proliferirajućih plovila kako bi se formirala shunts i aneurizma, što dovodi do dilatacije vena i pogoršanja hipoperfuzije mrežnice;
Fenomen povjerenja sa daljnjim napredovanjem ishemike, koji je uzrok formiranja infiltrata i ožiljaka;
Odvojen mrežnice kao rezultat njenog ishemijskog raspada i formiranja vitretarnih trakta;
Knorhage u staklastom tijelu kao rezultat hemoragičnih srčanih udara, masivne vaskularne invazije i ružing aneurizma;
Širenje plovila Irisa (dijabetičke rublje), što dovodi do razvoja sekundarnog glaukoma;
Makulopatija sa oticanjem oticanje.
Epidemiologija
Ostalo je najčešći uzrok sljepoće među radnoj populaciji razvijenih zemalja, te rizik od razvoja sljepoće kod pacijenata sa dijabetesom 10-20 puta veći nego u ukupnom stanovništvu. U vrijeme dijagnostike SD-1, DR ne otkrivaju gotovo bilo koji od pacijenata, nakon 5 godina, bolest se otkriva u 8% pacijenata, a sa trideset godina dijabetesa - u 98% Pacijenti. U vrijeme dijagnostike, DR SD-2 otkriven je u 20-40% pacijenata, a među pacijentima sa petnaest godina iskustva, SD-2 - u 85%. Na SD-1, proliferativna retinopatija zabrinuta je relativno češće, a na SD-2 - makulopatiju (75% slučajeva makulopatije).
Kliničke manifestacije
Prema općenito prihvaćenoj klasifikaciji, razlikuju se 3 faze dr.
(Tabela 7.18).
Dijagnostika
Kompletan oftalmološki pregled, koji uključuje direktnu oftalmoskopiju sa fotografiranjem mrežnice, prikazan je pacijentima sa SD-1 nakon 3-5 godina nakon manifestacije bolesti, a pacijenti sa SD-2 odmah nakon otkrivanja. U budućnosti se takva istraživanja moraju ponoviti godišnje.
Stol. 7.18.Klasifikacija dijabetičke retinopatije
 Diferencijalna dijagnoza
Diferencijalna dijagnoza
Ostala bolest oka kod pacijenata sa dijabetesom.
Tretman
Osnovni princip liječenja dijabetičke retinopatije, kao i druge kasne komplikacije, je optimalna nadoknada SD-a. Najefikasnija metoda liječenja dijabetičke retinopatije i sprečavati slijepilo laserska fotokoagulacija.Svrha
 Sl. 7.11.Dijabetička retinopatija:
Sl. 7.11.Dijabetička retinopatija:
a) neliferativno; b) nepolitički; c) Proliferativno
laserska fotokoagulacija je prestanak funkcioniranja novoformiranih plovila, koje predstavljaju glavnu prijetnju razvoju tako teških komplikacija, poput hemofta, udaraći mrežnice, trljanje iris i sekundarni glaukom.
Prognoza
Slijepoća se bilježi u 2% pacijenata sa CD-om (3-4% pacijenata sa SD-1 i 1,5-2% pacijenata sa SD-2). Približna frekvencija novih slučajeva sljepoće povezane sa DR iznosi 3,3 slučaja na 100.000 stanovnika godišnje. Tokom SD-1, smanjenje HbA1C-a na 7,0% dovodi do smanjenja rizika DR razvoja za 75% i smanjiti rizik od napredovanja za 60%. U SD-2, smanjenje HbA1C za 1% dovodi do smanjenja rizika od DR razvoja za 20%.
7.8.3. Dijabetička nefropatija
Dijabetička nefropatija(DNF) je definiran kao albuminurija (više od 300 mg albumina dnevno ili proteinuma više od 0,5 g proteina dnevno) i / ili smanjenje funkcije filtriranja bubrega u pojedincima sa CD-a u nedostatku mokraćnih infekcija , zatajenje srca ili druge bolesti bubrega. Microalbuminuria je definirana kao izlučivanje albumina 30-300 mg / dan ili 20-200 μg / min.
Etiologija i patogeneza
Glavni faktori rizika DNF-a su trajanje SD, hronične hiperglikemije, arterijske hipertenzije, dislipidemije, bubrežne bolesti od roditelja. Kada je DNF prvenstveno pogođen aparati za klasterbubreg.
1. Jedan od mogućih mehanizama za koji hiperglikemijapromovira razvoj lezije glomera, je nakupljanje Sorbitola zbog aktiviranja poliološkog staza metabolizma glukoze, kao i više od konačnih proizvoda od žiriranja.
2. Hemodinamičke kršenja, naime introlubok arterijska hipertenzija(podizanje krvnog pritiska unutar bubrežnih glomija) je najvažnija komponenta patogeneze
Uzrok intraclude hipertenzije je kršenje tona arteriole: širenje nastalog i sužavanje završetka.
Stol. 7.19.Dijabetička nefropatija
 To se, zauzvrat događa pod utjecajem niza humoralnih faktora, poput angiotenzina-2 i endotelina, kao i zbog kršenja elektrolitnih svojstava bazalne membrane Glomeruli. Pored toga, intrakralnotska hipertenzija doprinosi sistemskoj hipertenziji, što određuje većina pacijenata sa DNF-om. Zbog intrakralnobične hipertenzije, postoji oštećenje bazalnih membrana i filtracionih pora,
To se, zauzvrat događa pod utjecajem niza humoralnih faktora, poput angiotenzina-2 i endotelina, kao i zbog kršenja elektrolitnih svojstava bazalne membrane Glomeruli. Pored toga, intrakralnotska hipertenzija doprinosi sistemskoj hipertenziji, što određuje većina pacijenata sa DNF-om. Zbog intrakralnobične hipertenzije, postoji oštećenje bazalnih membrana i filtracionih pora,
preko kojeg tragovi počinju prodirati (MicroAlbuminuria),a zatim značajne količine albumina (proteinurija).Zadebljanje bazalnih membrana uzrokuje promjenu svojih svojstava elektrolita, što po sebi dovodi do veće količine albumina ultrafiltrate čak i u odsustvu veličine filtracijskog pora.
3. Genetska predispozicija.Rođaci pacijenata sa DNF-om sa povećanom frekvencijom događaju se arterijsku hipertenziju. Postoje podaci o vezi DNF-a s polimorfizmom gena ACE. Mikroskopski, za vrijeme DNF-a, zadebljanje bazalne membrane glodara, ekspanzija mezanygia, kao i vlaknastim promjenama koje donose i trajne arteriole otkrivaju se. U završnoj fazi, koja klinički odgovara hroničnom zatajenju bubrega (CPN), utvrđuje se fokus (Kimmelistil-Wilson), a zatim difuzne glomeroskleroze.
Epidemiologija
Microalbuminuria se određuje u 6-60% pacijenata sa SD-1 5-15 godina nakon njegove manifestacije. DNF je određeno za 35% od SD-1, češće kod muškaraca i ljudi koji su se razvili u dobi od 15 godina. U SD-2, DNF se razvija u 25% predstavnika evropske rase i u 50% azijske rase. Sveukupna rasprostranjenost DNF-a u SD-2 je 4-30%.
Kliničke manifestacije
Relativno rana klinička manifestacija, koja je indirektno povezana s DNF-om, arterijska hipertenzija. Ostale klinički eksplicitne manifestacije pripadaju kasnoj. Oni uključuju manifestacije nefrotičnog sindroma i hroničnog zatajenja bubrega.
Dijagnostika
Screening na DNF u osobama sa CD-om podrazumijeva godišnje testiranje na microalbuminuriasa SD-1 5 godina nakon manifestacije bolesti, a na SD-2 odmah nakon otkrijevanja. Pored toga, potrebno je barem godišnja definicija nivoa kreatinina za izračunavanje brzina glomerularne filtracije (SCF).SCF se može izračunati koristeći razne formule, na primjer, Cocroft-Golta Formula:
Za muškarce: a \u003d 1,23 (nop SCF 100 - 150 ml / min) za žene: a \u003d 1,05 (norma SCF 85 - 130 ml / min)
Na početnim fazama DNF-a može se otkriti povećanje SCF-a, što postepeno pada kao CPN razvijeno. Microalbuminuria počinje biti određen 5-15 godina nakon manifestacije SD-1; Sa SD-2 u 8-10% slučajeva nalazi se odmah nakon što se otkrije, vjerovatno zbog dužeg asimptomatskog toka bolesti do dijagnoze. Vrhunac razvoja eksplicitne proteinurije ili albuminurije na SD-1 pada između 15 i 20 nakon početka. Proteinurija svjedoči o. nepovratna stvarDNF, koji prije ili kasnije dovesti do CPN-a. Uremija je u prosjeku 7-10 godina nakon pojave eksplicitne proteinurije. Treba napomenuti da SCF ne korelira sa proteinurijom.
Diferencijalna dijagnoza
Ostali uzroci proteinurije i neuspjeha bubrega u pojedincima iz SD-a. U većini slučajeva, DNF se kombinuje sa arterijskom hipertenzijom, dijabetičkom retinopatijom ili neuropatijom, u kojem bi se diferencijalna dijagnoza trebala biti posebno temeljita. U 10% slučajeva, sa SD-1 i u 30% slučajeva, tokom SD-2, proteinurija nije povezana sa DNF-om.
Tretman
♦ Glavni uvjeti primarnog i srednjeg prevencija
DNF.su kompenzacija SD-a i održavanje normalnog sistemskog krvnog pritiska. Pored toga, primarna prevencija DNF-a podrazumijeva smanjenje potrošnje hrane proteina - manje od 35% dnevnog kalorage.
♦ u fazama microalbuminuriai proteinurijapacijenti su prikazani imenovanje ACE inhibitora ili blokatora angiotenzinskih receptora. Sa istodobnom arterijskom hipertenzijom, propisane su u hipotenzivnim dozama, ako je potrebno u kombinaciji s drugim hipotenzivnim lijekovima. U normalnom arterijskom pritisku, ovi lijekovi su propisani u dozama koje ne vode do razvoja hipotenzije. I ACE inhibitori (u SD-1 i SD-2) i blokatorima receptora angiotenzina (u SD-2) doprinose sprečavanju prelaska mikroalbuminurije u proteinuriju. U nekim slučajevima, na pozadini ove terapije, u kombinaciji s naknadom dijabetesa za ostale parametre, mikroalbuminurija se eliminira. Pored toga, počevši od faze mikroalbuminurije potrebno je
smanjenje potrošnje proteina je manje od 10% dnevne kalorage (ili manje od 0,8 grama po kg kilograma) i soli manje od 3 grama dnevno.
♦ u pozornici CPNpo potrebi je potrebna korekcija terapije šećerom. Većina pacijenata sa SD-2 mora biti prevedena u terapiju inzuline, jer kašika kumulacija nosi rizik od teške hipoglikemije. Većina pacijenata sa SD-1 ima smanjenje inzulina potrebe, jer je bubreg jedno od glavnih mjesta njenog metabolizma. Uz podizanje nivoa kreatinina u serumu do 500 μmol / l i više treba postaviti pitanje pripreme pacijenta na ekstraCorporeuralno (hemodijalizi, peritoneal dijalizi) ili metodu tretmana hirurškog (transplantacija bubrega). Transplantacija bubrega prikazana je na nivoima kreatinina do 600-700 μmol / l i smanjuju brzinu glomerularnog filtracije manja od 25 ml / min, hemodijalizi - 1000-1200 μmol / l i manje od 10 ml / min, odnosno manje od 10 ml / min.
Prognoza
U 50% bolesnika sa SD-1 i 10% sa SD-2, koji otkriva proteinuriju, CPN se razvija u narednih 10 godina. 15% svih smrtnih slučajeva pacijenta sa SD-1 mlađem od 50 godina povezano je sa CPN zbog DNF-a.
7.8.4. Dijabetička neuropatija
Dijabetička neuropatija(DN) je kombinacija sindroma lezija nervnog sistema, koja se može klasificirati ovisno o prevladinom uključenju u proces raznih odjela (senzorny, autonomna), kao i prevalencija i težina lezije (Tabela 7.20).
I. Senzomotor neuropatija:
Simetričan;
Fokusna (mononereropatija) ili polifokal (kranijalni, proksimalni motor, mononeroidni udovi i torzo).
II. Autonomna (vegetativna) neuropatija:
Kardiovaskularna (ortostatska hipotenzija, sindrom srčanog denengacije);
Gastrointestinalno (želudac, diskonezija bilijarnog trakta, dijabetička enteropatija);
Urogenitata (s oštećenim funkcijama mjehura i seksualne funkcije);
Kršenje u pacijentovoj sposobnosti da prepozna hipoglikemiju;
Kršenje funkcije učenika;
Kršenje funkcija znojnih žlijezda (distalna anhidroza, hiperhidroza prilikom jela).
Stol. 7.20.Dijabetička neuropatija
 Etiologija i patogeneza
Etiologija i patogeneza
Glavni uzrok dana je hiperglikemija. Pretpostavlja se nekoliko mehanizama njegove patogeneze:
Aktivacija poliolske staze metabolizma glukoze, kao rezultat čije Sorbitol, fruktoza i smanjenje mioindose i glutationa događaju se u nervnim ćelijama. To, zauzvrat dovodi do aktiviranja slobodnih radikalnih procesa i smanjujući nivo dušičnog oksida;
Ne-enzimski glikozilacija membrana i citoplazmatskih proteina nervnih ćelija;
Microaganiopatija vasa Nervorum,što dovodi do usporavanja kapilarne protok krvi i hipoksije živaca.
Epidemiologija
Prevalencija dno s obje vrste SD iznosi oko 30%. Sa SD-1 5 godina kasnije, počinje da se otkriva iz 10% pacijenata. Učestalost novih slučajeva dna u SD-2 je oko 6% pacijenata godišnje. Najčešća opcija je distalni dan simetričnog osjetitora.
Kliničke manifestacije
Senzomotor DN.manifestuju kompleksom motornih i osjetljivih poremećaja. Česti simptom distalnog oblika parestezijašto se manifestuje sa osjećajem "puzanja goosebumps", ukočenost. Pacijenti se često žale na glavu stopala, iako ostaju topli na dodir, što je znak koji omogućava razlikovanje polineeropatije iz ishemijskih promjena kada su stopala na dodir hladnu. Rana manifestacija senzorne neuropatije je kršenje osjetljivosti na vibraciju. Karakteristično je sindrom "nemirnog stopala", što je kombinacija noćne parestezije i visoke osjetljivosti. Bol u nogamaČešće zabrinute noću, dok ponekad pacijent može skinuti dodir pokrivača. U tipičnom slučaju boli, za razliku od takvog sa brisanjem bolesti, arterije se mogu smanjiti prilikom hodanja. Nakon godina, bol se može spontano prekinuti zbog smrti malih nervnih vlakana odgovornih za osjetljivost na bol. Hipoestezijamanifestuje se gubitkom osjetljivosti prema tipu "čarapa" i "rukavice". Kršenje dubokog, proprioceptivne osjetljivosti dovodi do kršenja koordinacije i poteškoće kretanja (senzorna ataksija). Pacijent se žali na "druga stopala", osjećaj "stojeći na pamuku". Kršenje trofične inerviranje dovodi do degenerativnih promjena u koži, kostima i tetivama. Kršenje osjetljivosti na bol dovodi do česte, a ne vidljive pacijenta sa zaustavljanjem Microtraummamm-a koji se lako zaraže. Kršenje koordinacije i šetnje dovodi do ne-fiziološke preraspodjele tereta na zglobovima stopala. Kao rezultat toga, poremećen je anatomski odnos u zakoničkom aparatu nogu.
Luk stopala je deformiran, oticanje, prelomi, razvijaju se kronični gnojleni procesi (vidi klauzulu 7.8.5).
Nekoliko oblika autonomnog dana. Prouzrokovati kardiovaskularni oblik- Oštećeno inerviranje kardiovaskularnog kompleksa i velikih plovila. Lutajući živac je najduži živac, u vezi s kojom je zadivljen prije drugih. Kao rezultat prevladavanja simpatičkih uticaja razvija se tahkardia počiva.Neadekvatan odgovor na ortostazu se manifestuje ortostatska hipotenzijai sinkopalne države. Vegetativno denervaranje plućnog kompleksa dovodi do nepostojanja varijabilnosti srčanog ritma. Uz autonomnu neuropatiju, povezana je povećana rasprostranjenost među pacijentima s miokardskim inkazacijama SD.
Simptomi gastrointestinalni oblikDani su gastroplaz s sporim ili, naprotiv, brzi prazan stomak, koji mogu stvoriti poteškoće u odabiru terapije inzulinom, jer je vrijeme i obim usisavanja ugljikohidrata nejasno variraju; Aton Esofagus, refluks-ezofagitis, disfagia; Proljev vode. Za urogenitalni oblikDno karakteriše atonija uretera i mjehura, što dovodi do sklonosti u mokraćnim infekcijama; Erektilna disfunkcija (oko 50% pacijenata sa SD); Retrogradna ejakulacija.
Ostale moguće manifestacije vegetativnog dana - kršenje sposobnosti prepoznavanja hipoglikemije, kršenje funkcije učenika, kršenje funkcija znojnih žlijezda (anhidroza), dijabetičara, dijabetičara.
Dijagnostika
Neurološki pregled pacijenata sa SD-om mora se provoditi godišnje. Na minimum, podrazumijeva testove usmjerene na identifikaciju neuropatije distalne senzorine. Za to se procjena osjetljivosti vibracije koristi se koristeći ocjenu Chateneneton, taktilna osjetljivost s monofilamentom, kao i temperaturne i osjetljivosti na bol. Prema svedočenju, studira se stanje vegetativnog nervnog sistema: za dijagnosticiranje insuficijencije parasimpatičke srčane inerviranje, koristi se brojni funkcionalni uzorci, poput mjerenja otkucaja srca s dubokim disanjem s evaluacijom varijabilnosti
srčani ritam i uzorak Waltasalva; Ortostatski uzorak koristi se za dijagnosticiranje insuficijencije simpatičnosti na unutrašnjosti srca.
Diferencijalna dijagnoza
Neuropatija druge geneze (alkoholna, uremička, sa 12 identična anemija, itd.). Dijagnoza disfunkcije jednog ili drugog organa kao rezultat vegetativne neuropatije uspostavljena je tek nakon isključenja organske patologije.
Tretman
1. Optimizacija terapije šećerom.
2. Njega za noge (vidi klauzulu 7.8.5).
3. Učinkovitost neurotropnih lijekova (α-lipoična kiselina) nije potvrđena u svim studijama.
4. Simptomatska terapija (anestezija, sigrana sa erektilnom disfunkcijom, floccortisis sa ortostatskom hipotenzijom itd.).
Prognoza
U početnim fazama, dan može biti reverzibilan prema pozadini kompenzacije stalak za SD. Dno se određuje u 80% pacijenata sa ulcerovnim lezijama i glavna je amputacija faktora rizika
7.8.5. Dijabetički sindrom stopala
Dijabetički sindrom stopala(SDS) - patološko stanje stopala na SD-u uz pozadinu štete na perifernim živcima, kožom i mekim tkivima, kostima i zglobovima i manifestuju sa akutnim i hroničnim ulsima, lezijama kostiju i gnojnim procesima ( Tabela 7.21).
Etiologija i patogeneza
Patogeneza SDS-a je multikomponentna i zastupljena je kombinacijom neuropatskih i perfuzijskih poremećaja s izraženom tendencijom do infekcije. Na osnovu prevladavanja patogeneze jednog ili drugog od navedenih faktora, 3 glavne oblike
Stol. 7.21.Dijabetički sindrom stopala
 I. neuropatski oblik(60-70 %):
I. neuropatski oblik(60-70 %):
Bez osteoarttropatije;
Sa dijabetičkom osteoarttropatijom.
II. Neuriecemic (miješani) obrazac(15-20 %).
III. Ishemijski oblik(3-7 %).
Neuropatski oblik SDS-a. U dijabetičkoj neuropatiji, distalni odjeli najduže živce utječu prije svega. Dugi deficit trofičkog impulsacije dovodi do hipoterofije kože, kostiju, ligamenata, tetiva i mišića. Rezultat hipotrofije spojnih struktura je deformacija stopala s nefiziološkom preraspodjelom referentnog opterećenja i njenog pretjeranog povećanja zasebnih područja. Na tim mjestima, na primjer, u području projekcijskog glava kostiju kosti, zadebljanje kože i formiranje hiperkeratoze. Stalni pritisak na ovim područjima dovodi do upalne autolize dovedenih mekih tkiva, što stvara preduvjete za formiranje ulcerovnog oštećenja. Kao rezultat atrofije i smetnje, koža postaje suha, lako je puknuti. Zbog smanjenja osjetljivosti na bol, pacijent često ne obraća pažnju na promjene koje se događaju. Ne može pravovremeno otkriti neugodnost cipela, što dovodi do formiranja tuša i kukuruza, ne primjećuje uvođenje stranih tijela, male rane na mjestima pucanja. Situacija pogoršava umanjenje duboke osjetljivosti, manifestovan je kršenjem hoda, nepravilnog snimka. Najčešće ulcerozna defekcija zaražena je stafilokokim, streptokokim, bakterijama crevne grupe; Često se pridružuje anaerobnoj flori. Neuropatska osteoarthrija rezultat je teških distrofičnih promjena u bonušem stopala (osteoporoza, osteoliza, hiperostoze).
Ishemijski SDS obrazac to je posljedica ateroskleroze arterija donjih ekstremiteta, što dovodi do kršenja glavnog protoka krvi, tj. To je jedna od varijanti dijabetičke makroaganipatije.
Epidemiologija
SDS se posmatra u 10-25%, a prema nekim podacima, u jednom ili drugom obliku, u 30-80% bolesnika sa dijabetesom. U SAD-u godišnja potrošnja na tretmanu pacijenata sa CD-ovima SD C su milijardu dolara.
Kliničke manifestacije
Za neuropatski oblikSDS izdvajaju dvije najčešće vrste lezija: neuropatski čir i osteoarttropatija (s razvojem
 Sl. 7.12.Neuropatski čir s sindromom nozi dijabetičara
Sl. 7.12.Neuropatski čir s sindromom nozi dijabetičara
 Sl. 7.13.Varcot spoj sa dijabetičkim sindromom stopala
Sl. 7.13.Varcot spoj sa dijabetičkim sindromom stopala
charco zglob). Neuropatski čir,obično, lokalizirano u regiji jedinog i intervala intervala, I.E. U odjeljcima stopala koji doživljavaju najveći pritisak (Sl. 7.12).
Destruktivne promjene uređaja za noge veziva mogu napredovati u više mjeseci i dovesti do teške deformacije kostiju - diabetic osteo arthropatijai formiranje charcot je zglobistovremeno, stopalo se formalno upoređuje sa "torbom sa kostima"
Za ishemijski oblik SDS-a
koža u nogama je hladna, blijeda ili cijanotika; Manje često ima ružičasto-crvenu nijansu širenja površnih kapilara kao odgovor na ishemiju. Ulcerovativni nedostaci nastaju prema vrsti atralne nekroze - na vrhovima prstiju, rubnu površinu potpetica (Sl. 7.14).
Puls na arterijama stopala, poplitealne i bedrene arterije su oslabljene ili ne palpable.
U tipičnim slučajevima pacijenti nameću žalbe "presijecanjem hroma". Težina ishemijskih lezija udova određena je tri glavna faktora: težina stenoze, razvoj kolateralnog protoka krvi, uvjet koagulacije krvi.
Dijagnostika
Pregled stopala pacijenta SD-a trebalo bi se izvršiti svaki put tokom posjete ljekaru, a ne manje od jednom u pola godine. Dijagnostika SDS-a uključuje:
 Sl. 7.14.Akralna nekroza sa ishemijskim oblikom sindroma dijabetičkog stopala
Sl. 7.14.Akralna nekroza sa ishemijskim oblikom sindroma dijabetičkog stopala
Inspekcija nogu;
Evaluacija neurološkog statusa - razne vrste osjetljivosti, refleksi tetiva, elektromiografija;
Procjena stanja arterijskog protoka krvi - angiografija, doplerometrija, doplerography;
Rendgenski snimak stajališta i zglobova gležnja;
Bakteriološki pregled ispuštanja rane.
Diferencijalna dijagnoza
Izvodi se s procesima rana u koracima druge geneze, kao i ostale okluzivne bolesti plovila donjih ekstremiteta i patologiju spojeva stopala. Pored toga, klinički oblici SDS-a moraju se razlikovati (tablica 7.22).
Tretman
Tretman neuropatski zaraženobrasci SDS-a uključuju kompleks sljedećih događaja:
Optimizacija kompenzacije CD-a u pravilu, povećanje doze inzulina i sa SD-2 - prenošenje na njega;
Sistemska terapija antibioticima;
Potpuno istovar stopala (to može uzrokovati zacjeljivanje čira u roku od nekoliko tjedana);
Lokalna obrada rana uklanjanja hiperkeratoza;
Briga o nogama, ispravan izbor i nošenje posebnih cipela. Pravovremena provedena konzervativna terapija omogućava
izbjegavajte operativnu intervenciju u 95% slučajeva.
Stol. 7.22.Diferencijalna dijagnoza kliničkih obrazaca SDS-a
 Tretman ishemičansDS obrasci uključuju:
Tretman ishemičansDS obrasci uključuju:
Optimizacija kompenzacije CD-a u pravilu, povećanje doze inzulina i sa SD-2 - prenošenje na njega;
U nedostatku čirlovskih nekrotičnih lezija, ergoterapija (1-2 sata hodanja dnevno doprinose razvoju kolateralnog protoka krvi);
Operacije revaskularizacije na pogođenim plovilima;
Konzervativna terapija: antikoagulansi, aspirin (do 100 mg / dan), ako je potrebno - fibrinolitici, pripreme prostaglandina E1 i prostacticlin.
U razvoju opsežnih gnojnih nekrotičnih lezija, sa svim VDS varijantima podiže se amputacija.
Prognoza
Od 50 do 70% od ukupnog broja agitacije stopala, a pacijentima obrađuju dijabetes. Amputacija stopala kod pacijenata sa SD-om proizvodi se 20-40 puta češće od onih bez dijabetesa.
7.9. Šećerni dijabetes i trudnoća
Gestacijske dijabetes(GSD) je kršenje tolerancije glukoze, prvi put otkrivenim tokom trudnoće (Tabela 7.23). Ova definicija ne isključuje da bi patologija razmjene ugljikohidrata mogla prethoditi početku trudnoće. GHS bi se trebalo razlikovati od situacija kada je žena sa dijagnosticiranim dijabetesom (vršnjakom starosti, češće od SD-1) trudnoća.
Etiologija i patogeneza
GES je sličan onima u SD-2. Visok nivo jajnika i placentalnog steroida, kao i povećanje formiranja kortizola nadbubrežnog korteksa vodi tokom trudnoće do razvoja fiziološkog izolinskog otpora. Razvoj DVS-a povezan je sa činjenicom da se inzulin otpor, prirodno razvija tokom trudnoće, a dakle, povećana potreba za inzulinom u predisponiranim osobama prelazi funkcionalnu sposobnost β-ćelija PJZ-a. Nakon isporuke uz povrat hormonalnih i metaboličkih odnosa na početni nivo, obično prolazi.
Stol. 7.23.Gestacijske dijabetes
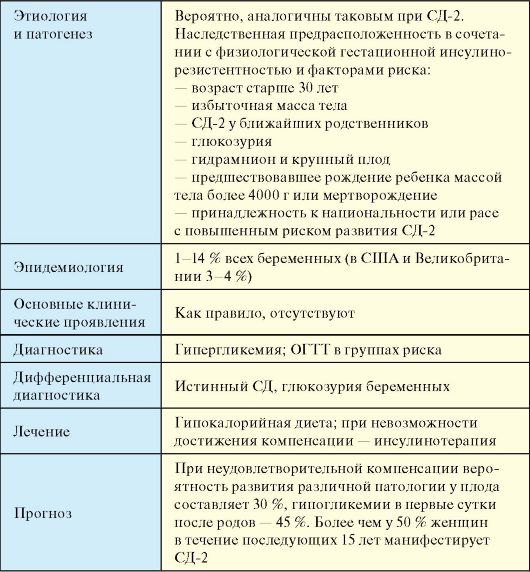 GSD se obično razvija u sredini 2 tromjesečje, između 4 i 8 mjeseci trudnoće. Velika većina pacijenata ima višak tjelesne težine i povijest opterećene AE. Faktori rizika GDG-a, kao i grupe žena s niskim rizikom razvoja DVS-a, prikazani su u tabeli. 7.24.
GSD se obično razvija u sredini 2 tromjesečje, između 4 i 8 mjeseci trudnoće. Velika većina pacijenata ima višak tjelesne težine i povijest opterećene AE. Faktori rizika GDG-a, kao i grupe žena s niskim rizikom razvoja DVS-a, prikazani su u tabeli. 7.24.
Stol. 7.24.Faktori rizika za razvoj gestacijskog dijabetesa
 Majka hiperglikemija dovodi do hiperglikemije u sistemu cirkulacije krvi djeteta. Glukoza lako prodire u placenu i kontinuirano se kreće u plod majčine krvi. Takođe se pojavljuje aktivni prevoz aminokiselina i prenos ketonnih tela voća. Za razliku od ovog inzulina, glukagona i besplatnih masnih kiselina majke u krvi fetusa ne padnu. U prvih 9-12 tjedana trudnoće, PJZ fetal još nije proizveo vlastiti inzulin. Ovaj put odgovara fazi fetalnog organogeneze, kada se na stalnu hiperglikemiju majke mogu formirati različite malformacije razvoja (srce, kralježnicu, kičmeni moždini, gastroniju). Od 12. sedmice trudnoće, PJZ fetal počinje sintetizirati inzulin, a u odgovoru na hiperglikemiju, reaktivne hipertrofije i hiperplazija β-ćelija fetalnog pJz razvijaju se. Zbog hiperinsulinmije, makronaredbe ploda se razvija, kao i ugnjetavanje iz lecithinske sinteze, što objašnjava visoku frekvenciju razvoja disajnih nevolja u novorođenčadi. Kao rezultat hiperplazije β-ćelija i hiperinsulinmije pojavljuje se tendencija teške i duge hipoglikemije.
Majka hiperglikemija dovodi do hiperglikemije u sistemu cirkulacije krvi djeteta. Glukoza lako prodire u placenu i kontinuirano se kreće u plod majčine krvi. Takođe se pojavljuje aktivni prevoz aminokiselina i prenos ketonnih tela voća. Za razliku od ovog inzulina, glukagona i besplatnih masnih kiselina majke u krvi fetusa ne padnu. U prvih 9-12 tjedana trudnoće, PJZ fetal još nije proizveo vlastiti inzulin. Ovaj put odgovara fazi fetalnog organogeneze, kada se na stalnu hiperglikemiju majke mogu formirati različite malformacije razvoja (srce, kralježnicu, kičmeni moždini, gastroniju). Od 12. sedmice trudnoće, PJZ fetal počinje sintetizirati inzulin, a u odgovoru na hiperglikemiju, reaktivne hipertrofije i hiperplazija β-ćelija fetalnog pJz razvijaju se. Zbog hiperinsulinmije, makronaredbe ploda se razvija, kao i ugnjetavanje iz lecithinske sinteze, što objašnjava visoku frekvenciju razvoja disajnih nevolja u novorođenčadi. Kao rezultat hiperplazije β-ćelija i hiperinsulinmije pojavljuje se tendencija teške i duge hipoglikemije.
Epidemiologija
CD pati od 0,3% svih žena reproduktivnog doba, 0,2-0,3% trudnica već je u početku bolesno, a za 1-14% trudnoće, GSD razvija ili manifestuje istinski SD. Prevalencija SDS-a varira u različitim populacijama, tako da je u SAD-u otkriveno u oko 4% trudnica (135 hiljada slučajeva godišnje).
Kliničke manifestacije
Sa GPS-om nedostaju. Možda postoje određeni simptomi dekompenzacije SD-a.
Dijagnostika
Određivanje nivoa glukoze u krvi na prazan stomak prikazano je svim trudnicama unutar biohemijskog testa krvi. Žene koje pripadaju grupi rizika (Tabela 7.24), pokazuju test oralnog glukoze(OGTT). Mnogo je opcija za svoje trudnice. Najlakši od njih podrazumijeva sljedeća pravila:
3 dana prije ispitivanja, žena je na običnom prehranu i pridržava se uobičajene fizičke aktivnosti;
Test se izvodi ujutro na prazan stomak, nakon noćnog gladi, najmanje 8 sati;
Nakon uzimanja uzorka krvi, prazna ženka pije rastvor za 5 minuta, sastoji se od 75 grama suhe glukoze raspuštene u 250-300 ml vode; Ponovno određivanje nivoa glikemije obavlja se nakon 2 sata.
Dijagnoza GSD-a postavljena je na sljedeće kriteriji:
Glukoza puna krv (venski, kapilarni) prazan stomak\u003e 6.1 mmol / l ili
Glukoza plazma venske krvi ≥ 7 mmol / l ili
Glukoza čvrsta kapilarna krv ili plazma venske krvi 2 sata nakon opterećenja 75 g glukoze ≥ 7,8 mmol / l.
Ako žena koja pripada grupi rizika, rezultati studije odgovaraju normi, test se ponovo koristi na 24-28 tjedan trudnoće.
Diferencijalna dijagnoza
GSD i istinski SD; Glukosurija trudnica.
Tretman
Rizik za majku i plod, kao i pristupi tretmanu SD-a i karakteristikama kontrole nad njim s BDG-om i sa istinskim SD-om su isti. Kasne komplikacije SD-a tijekom trudnoće mogu značajno napredovati, ali uz visokokvalitetnu nadoknadu za SD indikacije za prekid trudnoće. Žena koja pati od SD-a (u pravilu govorimo o SD-1), trebala bi planirati trudnoću u mladosti kada je rizik od najnižeg rizika. Ako se planira trudnoća, preporučuje se otkazati kontakt
uhvatiti nekoliko mjeseci nakon postizanja optimalne nadoknade. Kontraindikacije za planiranje trudnoće su ozbiljne nefropatije sa progresivnim zatajenjem bubrega, teškim CD-ovima, teškom proliferativnom retinopatijom, ne-korekcijom, ketoacidozom u ranoj trudnoći (ketone tijela su teratogeni faktori).
Svrha liječenjaGSD i istinski SD tokom trudnoće je postizanje sljedećih laboratorijskih pokazatelja:
Spool Glycemia< 5-5,8 ммоль/л;
Glikemija 1 sat nakon jela< 7,8 ммоль/л;
Glikemija 2 sata nakon obroka< 6,7 ммоль/л;
Prosječna vrijednost dnevnog glikemijskog profila< 5,5 ммоль/л;
HBA1C nivo sa mjesečnim nadzorom, poput zdravih (4-6%).
Sa SD-1, van trudnoće, žena bi trebala dobiti intenzivnu inzulinu terapiju, ali nivo glikemije tokom trudnoće preporučuje se ocjenjivati \u200b\u200b7-8 puta dnevno. Ako je nemoguće postići opojmaću opozivu u pozadini običnih injekcija, potrebno je razmotriti prijevod pacijenta na terapiju inzulinom pomoću inzulinskog raspršivača.
U prvoj fazi liječenje GSD-adijetalna terapija je dodijeljena, koja se sastoji od ograničavanja dnevne kaloražom od oko 25 kcal / kg stvarne težine, prije svega zbog najlakših ugljikohidrata i životinjskih masti, kao i širenje fizičkog napora. Ako je protiv pozadine dijetalne terapije, nije moguće postići ciljeve liječenja, pacijent mora biti dodijeljena intenzivna inzulinska terapija. Bilo koji tabletski lijekovi šećera (TSP) tokom trudnoće kontraindiciran.Ispada da je inzulin terapija potrebna za prevođenje oko 15% žena.
Prognoza
Uz nezadovoljavajuću nadoknadu DV-a i SD-a tokom trudnoće, vjerojatnost razne patologije u fetusu je 30% (rizik je 12 puta veći nego u ukupnom stanovništvu). Više od 50% žena, koje su tokom trudnoće, otkriveno GDS, za narednih 15 godina manifestuje SD-2.
U prevenciji višefaktorijalnih bolesti sa nasljednom predispozicijom, na koji je EDF potrebna vezamedicinsko i genetsko savetovanje. Glavni zadatak medicinske i genetske konsultacije je utvrditi genetski rizik od bolesti i objasniti njegovo značenje u pristupačnom obliku. Kada su SD u medicinski i genetski savjet najčešće ovisni o procjeni rizika od bolesti u budućoj djeci zbog prisutnosti ove bolesti u prethodnoj djeci, ili među supružnicima i / ili samim rođacima.Stanovništvo-genetske studije dozvoljene su da to izračunaju doprinos genetskih faktora u razvoju SD sastavlja 60-80%. S tim u vezi, početna relevantnost i budućnost stječe medicinsko i genetsko savjetovanje rođaka pacijenata sa SD-om.
Glavna pitanja sa kojima se obično morate suočiti sa liječnikom odnose se na rizik od razvoja SD-a imati više djece ili sestara braćepacijent, sposobnost da ga klasificirate prognoza u Titusažimanje budućih (planiranih) članova porodice.
Konsultantske porodice pacijenata sa pacijentima vrste tipa 1 sastoji se od nekoliko opšte prihvaćenih faza koji imaju svoje karakteristike za ovaj kontingentni.
11.1. Faze savjetovanja
Prva faza savjetovanja - Sažetak dijagnoze bolesti.
Obično dijagnoza dijabetesa tipa 1 u dječje i mladenačku dob ne predstavlja poteškoće. Međutim, u prisustvu SD-a, ostali članovi porodice trebaju provjeru vrste dijabetesa koji u nekim slučajevima može doći do teških zadataka i zahtijevat će liječnik da pažljivo prikupi anamnezu rođaka pacijenta. Diferencijalna dijagnoza između dvije glavne vrste SD (1 i 2) vrši se prema općenito prihvaćenim kriterijima.
Dokazano sa opsežnim studijama stanovništva genetska heterogenost dviju glavnih vrsta SD-a svjedoči o svojoj nosološkoj neovisnosti i neovisnosti nasljeđivanja. To znači da su oni dostupni u rodovničkim pojedinim pacijentima sa CD 2 tipom nasumični i ne bi se trebali uzeti u obzir prilikom procjene porodičnog rizika.
Prilikom provođenja medicinskog i genetskog savjetovanja također je potrebno isključiti genetski sindrome koji uključuju dijabetes melitus, jer ih karakterizira monogenični nasljedstvo.
Druga faza savjetovanja - Određivanje rizika od razvoja bolesti u pogledu dostupnih članova porodice i planiranim potomstvom potomstva.
Empirijske metode dobivene su prosječnom procjenom rizika od dijabetesa za članove porodica sa rodbinom sa tipom 1 SD. Maksimalni rizik ima rodbinu I stepena srodstva (djeca, roditelja, sestra braće) - u prosjeku od 2,5-3% na 5-6%. Utvrđeno je da frekvencija bolesti dijabetesa djeca od očeva sa SD 1 tipa 1 -2% većanego od majki s tipom 1.
U svakoj specifičnoj porodici rizik od razvoja bolesti ovisi o mnogim faktorima: broj pacijenata i zdravih rođaka, starosti manifestacije dijabetesa u članovima porodice, dob savjetovanja, itd.
Tabela 8.
Empirijski rizik za rodbinu pacijenata SD tipa 1
Na posebnoj tehnici se izračunavaju razvoj tablica rizikaSD 1. Tip ovisno o broju pacijenata i zdravih rođaka i dob konsultovane za porodice različitih vrsta. Obitelji, status roditelja i broj pacijenata sa SIBS-om predstavljeni su u tablici 9.
Dolje sindrom nije bolest, ova patologija je nemoguće spriječiti i izliječiti. Fetus s Downovim sindromom u 21. par kromosoma postoji treći dodatni kromosom, kao rezultat njihovog iznosa nije 46, ali je 47. Down sindrom opažen u jednoj od 600-1000 novorođenčadi od žena u dobi od 35 godina. Razlog zašto se to događa da nije u potpunosti razjašnjeno. Doktor iz Engleske John Langdon dole prvi je opisao ovaj sindrom 1866. godine, a 1959. francuski profesor Lezhen dokazao je da je to zbog genetskih promjena.
Poznato je da djeca s pola kromosoma stiču od majke, a polovina - od oca. Budući da ne postoji nijedna efikasna metoda liječenja sindroma, bolest se smatra neizlječivam, možete poduzeti mjere i ako želite roditi dijete zdravo, obratite se medicinskim i genetskim savjetima, gdje na temelju hromozoma Analiza, roditelji će biti odlučni, dijete će se roditi zdravo ili s Downovim sindromom.
Nedavno se takva djeca rađaju češće, oni su ga povezuju sa kasnim brakom, sa planiranjem trudnoće u dobi od 40 godina. Također se vjeruje da ako baka rodi kćerku nakon 35, tada se unuci mogu roditi s Downovim sindromom. Iako je prenatalna dijagnoza složen proces ankete, njegova je implementacija vrlo potrebna kako bi se mogla prekinuti trudnoću.
Šta je Down sindrom. Obično se može popraviti kašnjenjem razvoja motora. Takva djeca imaju urođene srčane nedostatke, patologiju razvoja gastrointestinalnog trakta. 8% pacijenata s Downovim sindromom su bolesna leukemija. Medicinski tretman može potaknuti mentalne aktivnosti, normalizovati hormonalnu neravnotežu. Uz pomoć postupaka fizioterapije, masaže, terapeutske gimnastike, možete pomoći djetetu da stiče vještine potrebne za samoposluživanje. Downov sindrom povezan je s genetskom kršenjem, ali ne vodi uvijek do kršenja fizičkog i mentalnog razvoja djeteta. Takva djeca, a u budućim odraslim osobama mogu sudjelovati u svim sferama života, neki od njih postaju glumci, sportaši i mogu se baviti javnim poslovima. Kako će se osoba razviti s ovom dijagnozom, u velikoj mjeri ovisi o okolišu u kojem raste. Dobri uvjeti, ljubav i njegu doprinose punopravnom razvoju.
Tabela rizika od sindroma Dowon, prema dobi
Verovatnoća Downovog sindroma zavisi od starosti majke, ali može se otkriti genetskim testom u ranim fazama trudnoće, a u nekim slučajevima ultrazvuk. Verovatnoća o dečijem sindromu po rođenju je niža nego u ranijim fazama trudnoće, jer Neki voće s Downovim sindromom ne preživljavaju.

Koji se rizik smatra niskim, a šta je visoko?
U Izraelu se rizik od sindroma dolje smatra visokim, ako je veći od 1: 380 (0,26%). Svi koji su u ovoj rizičnoj grupi treba provjeriti poltove vode. Ovaj rizik je jednak riziku za one žene koje su trudne u dobi od 35 godina i više godina.
Rizik je niži od 1: 380 smatra se niskim.
Ali mora se imati na umu da ove granice mogu plutati! Na primjer, u Engleskoj se smatra da je visok nivo rizika veći od 1: 200 (0,5%). To je zbog činjenice da neke žene smatraju rizik od 1 do 1000 - visokih, a ostalih 1 do 100 - nisko, jer sa takvim rizikom imaju šansu za rođenje zdravog djeteta jednako 99%.
Faktori rizika Down sindrom, Edwards, Patau
Glavni faktori rizika su dob (posebno značajno za Downov sindrom), kao i utjecaj zračenja, nekih teških metala. Treba imati na umu da čak i bez faktora rizika, voće može imati patologiju.
Kao što se vidi iz grafikona, ovisnost o riziku od starosti od starosti najznačajniji je za Downov sindrom, a manje značajan za još dvije trisomije:

Projekcija rizika od Downovog sindroma
Do danas, sve trudnice, pored oslanjajućih analiza, preporučuje se da se provede ispitivanje probira kako bi se utvrdio stepen rizika od sindroma rođenom djeteta i urođenih predizbova. Najproduktivnija anketa javlja se u 11 tjedana + 1 dan ili u sedmici 13 + 6 dana sa kokicom-tamom embriona od 45 mm do 84 mm. Trudnica može proći anketu i koristiti određeni ultrazvuk za to.
Prečlanija dijagnoza vrši se korištenjem biopsije zorionske vanene i proučavanja amnionske tekućine, koja je zatvorena posebnom iglom direktno iz mjehurića voća. Ali svaka žena treba znati da su takve metode konjugiraju s rizikom od krivičnih komplikacija poput pobačaja, fetalne infekcije, razvoj gubitka sluha u djetetu i još mnogo toga.
Kompletan kombinirani skrining I - II tromjesečje trudnoće omogućava vam identifikaciju urođenih malformacija na plodu. Šta uključuje ovaj test? Prvo, potrebna je ultrazvučna studija za 10-13 tjedana trudnoće. Izračun rizika vrši se kako bi se utvrdilo prisustvo nosne kosti, širine cervikalnog preklopa ploče, gdje se potkožna tečnost nakuplja u prvoj tripeziji trudnoće.
U sekundi, test krvi uzima se na horioljubinom gonadotropinu za 10-13 tjedana i na alfa fetoproteinu za 16-18 sedmica. Podaci kombiniranog pregleda obrađuju se posebnim računarskim programom. Naučnici su predložili novu metodologiju skrininga - kombinirajući evaluaciju rezultata dobivenih tokom studija u prvom i u drugim tromjesečjima. To nam omogućava da osiguramo jednu procjenu rizika od pojave sindroma dolje tokom trudnoće.
Za prvo tromjesečje koriste se rezultati određivanja RARR-a i mjerenja debljine prostora ogrlica, a za drugo tromjesečje - kombinacije AFP-a, ne-konjugiranog estriola, xg i inhibin-a koriste se. Upotreba integralne procjene za istraživanje probira omogućava nakon invazivnih intervencija za smanjenje frekvencije prekida trudnoće za voće sa normalnim kariotipom prema rezultatima citogenetskih dijagnostika.
Integralno i biohemijsko testiranje za probir Down sindrom omogućava vam dodatno identificiranje više slučajeva hromozomalnih anomalija. To doprinosi prevenciji nepoželjnih prekida trudnoće koji proizlaze iz Amniocentes ili Biopsy Vorsin horiona.
Stručni urednik: Mochalov Pavel Alexandrovich | d. n. terapeut
Obrazovanje: Moskovski medicinski institut. I. M. Sechhenov, specijalitet - "Terapeutski slučaj" 1991. godine, 1993. "Profesionalne bolesti", 1996. "terapija".
Genetika dijabetesa
Predviđanje tipa 1 SD 1 u visoko rizičnim grupama
T.V.NIKONOVA, I.I. Djed, Ji.p. Alekseev, M.N. Boldyreva, O.M. Smirnova, I.V. Dubinkin *.
Endokrinološki znanstveni centar I (jelen. Ramn I. I. Devov) Ramna, I * SSC "Institut za imunologiju" I (jelen. - ACAD. Ramna P.M. Khaitov) M3 Ruske Federacije, Moskva. Ja
Trenutno postoji povećanje učestalosti SD 1 širom svijeta. To je zbog više faktora, uključujući povećanje životnog vijeka pacijenata sa dijabetesom zbog poboljšanja dijagnostičke i terapijske pomoći, poboljšane plodnosti i pogoršanja ekoloških situacija. Smanjiti učestalost SD-a može se provesti preventivnim mjerama, predviđanjem i sprečavanjem razvoja bolesti.
Predispozicija za vrstu SD 1 genetski je određena. Incidencija tipa 1 tipa 1 kontrolira se niz gena: inzulin gen na hromosomu 11p15.5 (yuom2), geni na hromosomu \\\\ c (yuom4), 6t (yuom4), 6t (yuom4). Najveća važnost poznatih genetskih markera tipa 1 tipa 1 su geni regije NAA na kromosomu 6p 21.3 (SEZ1); Do 40% genetske predispozicije prema tipu SD 1 povezane su s njima. Nijedno drugo genetsko područje ne određuje rizik od razvoja bolesti uporediv sa na.
Visoki rizik od razvoja tipa 1, određuje se alelne varijante nuklearnih gena: 1 * 03, * 04; OOA1 * 0501, * 0301, OOB1 * 0201, * 0302. 95% pacijenata sa 1 vrstom SD-a ima AMA * 3 ili 011 * 4 antigena, a od 55 do 60% imaju i antigen. Allel Oob1 * 0602 retko se nailazi na vrstu tipa 1 i smatra se protestima.
Kliničke manifestacije dijabetesa prethodi latentnim periodom, karakterizira se prisustvom ostrvske mobilne markere za imunitet; Ti su markeri povezani s progresivnim uništavanjem.
Stoga su za članove porodice sa prethodnim slučajevima bolesti tipa SD 1, predviđanje bolesti posebno je važno.
Svrha ovog rada bila je formiranje razvojnih grupa visokog rizika u ruskom stanovništvu Moskovskog stanovništva na osnovu proučavanja genetskih, imunoloških i metaboličkih markera dijabetesa koji koriste porodični pristup.
Metode materijala i istraživanja
Anketirao 26 porodica u kojima jedan od roditelja bolesni 1 tipa SD 1, od kojih 5 su "nuklearne" porodice (samo 101 ljudi). Broj anketiranih članova porodice kretao se u rasponu od 3 do 10 osoba. Pacijenti SD 1 Vrsta očeva - 13, pacijenti sa mat 1 Vrsta majki su takođe 13. Obitelji u kojima bi oba roditelja bila bolesna 1 tipa, nije bilo.
Anketirao je 37 potomci pacijenata sa tipom SD 1 bez kliničkih manifestacija bolesti, od kojih je 16 -gen-roda, 21. male. Starost ispitanih potomci kretala se u rasponu od 5 do 30 godina. Distribucija ispitanih potomci prema dobi predstavljena je u tabeli. jedan.
Tabela 1
Starost anketirane djece (potomci)
Starost (godina) broj
U porodicama sa pacijentima sa majkama SD-a ispitivano je 17 djece (8 djevojaka, 9 dječaka), u porodicama sa pacijentima sa ocima dijabetesa - 20 djece (8 djevojčica, 12 dječaka).
Autoantililni agent (3 ćelije (ICA) određeno je na dva načina: 1) na kriozu gušterače muškarca I (0) krvnih grupa u reakciji indirektne imunofluorescencije; 2) U Istetestu "Istelettest" firma "Biomerica". Autoantitijelo za inzulin (IAA) određen je u enzimskom testu "IsleTtest" biomerici. Definicija antitijela na DGC izvedena je koristeći standardne setove "Dijalata anti-gada" kompanije "Boehringer Mannheim".
Definicija C-peptida izvedena je pomoću standardnih skupova kompanije "Sorrin" (Francuska).
HLA-kucanje pacijenata sa SD-om i njihovim porodicama izvedeno je na tri gena: DRB1, DQA1 i DQB1 od strane bolesničkog specifikacija - "" CIPHIJSKIM KORIŠTENJE koristeći lanac za polimerazu (PCR).
Izdanje DNK iz perifernih krvnih limfocita izvedeno je prema metodi R. Higuchi N. Erlich (1989) s nekim izmjenama: 0,5 ml krvi uzete sa EDTA, pomiješanim u 1,5 ml mikrocentrifuge cijevi kao što su eppendorf sa 0,5 ml lizirajući Rješenje koje se sastoji od 0,32 m Scrose, 10 mm - NS1 pH 7,5, 5 mm MGC12, 1% TRITONE X-100, centrifugirano za 1 min na 10.000 obrtaja, supernatant je uklonjen, a sedimenti ćelijskih jezgara 2 puta oprane sa Navedeni međuspremnik. Naknadna proteoliza izvedena je u 50 μl pufernog otopina koja sadrži 50 mm KCI, 10 mm TRI-NS1 pH 8.3, 2,5 mm MGCI2, 0,45% NP-40, 0,45% Twin-20 i 250 μg / ml proteinaze K na 37 "C 20 minuta. Inaktivirana proteinaza za grijanje u čvrstom stanjem termostatu na 95 "C za 5 minuta. Rezultirajući uzorci DNK odmah su korišteni za kucanje ili pohranjene na -20 "S. DNK koncentracija definirana od strane
fluorescencija sa Hoechst 33258 na DNK fluorimetrom (hoefer, USA), u prosjeku 50-100 μg / ml. Ukupno vrijeme izolacijskog postupka DNK iznosilo je 30-40 minuta.
PCR je izveden u 10 μl reakcijske smjese koja sadrži 1 μl DNK uzorka i sljedeće koncentracije preostalih komponenti: 0,2 mm svake DNTF (DATF, DTTF, DTTF i DGTF), 67 mm TRIS-HCL PH \u003d 8.8, 2.5 MM MGC12, 50 mm Nacl, 0,1 mg / ml želatin, 1 mm 2-mercaptoetanol, kao i 1 jedinicu termostabilna DNK polimeraza. Da bi se spriječilo promjene koncentracija komponenti reakcijske smjese zbog formiranja kondenzata, reakcijska smjesa bila je prekrivena 20 μl mineralnog ulja (Sigma, SAD).
Pojačalo je provedeno u termičkom biciklu MS2 (DNK tehnologiju JSC, Moskva).
Upisivanje LOCUS DRB1 izvedeno je u 2 faze. Tokom 1. kolu, genomski DNK je pojačan u dvije različite cijevi; U prvoj testnoj cijevi, primijeni se pojačavaju svi poznati aleli gena DRB1, u 2. paru temeljnih pripravnika, a pojačavaju samo aleli uključene u DR3, DR5, DR6, DR8 grupe, DR6, DR8 Grupe. U oba slučaja, temperatura pojačanja (za termociklor "MS2" sa aktivnim propisom) bila je sljedeća: 1) 94 ° C - 1 min; 2) 94 ° C - 20 C (7 ciklusa), 67 "C - 2 C; 92 "C - 1 C (28 ciklusa); 65 ° C - 2 s.
Dobiveni proizvodi razvedeni su 10 puta i koriste se u 2. kolu u sljedećem temperaturnom režimu: 92 "C - 1 C (15 ciklusa); 64 ° C - 1 s.
Upisivanje DQA1 lokusa izvedeno je u 2 faze. U prvoj fazi korišteni su par prajmera koji pojačava svu specifičnost DQA1 locusa, na 2. - parovima temeljnih slojnika, specifičnosti amplitude-ficiziranja * 0101, * 0102, * 0103, * 0201, * 0301, * 0401, * 0501, * 0601.
Prva faza izvedena je prema programu: 94 "C - 1 min; 94 ° C - 20 C (7 ciklusa), 58 "C - 5 C; 92" C - 1 C, 5 C (28 ciklusa), 56 "C - 2 s.
Proizvodi pojačanja 1. faze bili su razvedeni 10 puta i koriste se u 2. fazi: 93 "C - 1 C (12 ciklusa), 62" C - 2 s.
Upisivanje DQB1 lokusa također je provedeno u 2 etaže; Par Primera koji pojačava svu specifičnost DQB1 lokusa, temperaturni režim je sljedeći: 94 "C - 1 min.; 94 ° C - 20 s. (7 ciklusa); 67 ° C - 5 s.; 93 ° C - 1 C (28 ciklusa); 65ls - 2 str.
Druga faza rabljeni parovi temeljnika, specifičnosti za pojačavanje: * 0201, * 0301, * 0302, * 0303, * 0304, * 0305, * 04, * 0501, * 0502, * 0503, * 0601, * 0602/09; Proizvodi 1. faze bili su razvedeni 10 puta i pojačani u režimu: 93 "C - 1 s. (12 ciklusa); 67" C - 2 s.
Identifikacija proizvoda pojačanja i njihova dužina izvedena su u ultraljubičastoj svjetlosti (310 Nm) nakon elektroforeze 15 minuta ili 10% Paaga, 29: 1 na naponu od 500V ili u 3% agaroza na naponu od 300 V (u Oba su slučaja, kilometraža bila 3-4 cm) i bojenje s bromidom etidijem. Kao marker duljine, korišten sam PUC19 PLASMID PUC19 Restrictase MSP.
Rezultati i njegova rasprava
Utvrđeno je da su u 26 porodica iz 26 pacijenata sa 1 vrstama roditelja 23 osobe (88,5%) prevoznici povezani sa DRB1 * 05-DQA1 * 0501 - DQB1 * 0201 povezan sa DQB1 * 0201 - DQB1 * 0201; DRB1 * 04-DQAL * 0301-DQB 1 * 0302 ili njihove kombinacije (Tabela 2). U 2 pacijenta u genotipu postoji alel DQB 1 * 0201, povezan s vrstom tipa 1; Samo 1 pacijent ove grupe otkrio je genotip DRB1 * 01/01 koji
Distribucija genotipova među pacijentima sa tipom roditelja SD 1
01? 1 4/4 2 E1? U 1 - - - -
Ukupno 23 (88,5%) ukupno 3
0í? B1-ROA-RO Gaplotip otkrivene od strane anketiranih osoba
oogví ooi r)
ry sa studijama stanovništva nije bila povezana s vrstom tipa 1, nismo dodijelili podtipovi B1 * 04, iako polimorfizam ovog lokusa može utjecati na rizik od tipa 1 SD.
U genotipiziranju neposrednih potomci pacijenata sa tipom 1, otkriveno je da je od 37 ljudi 30 (81%) naslijeđeno povezano sa SD 1 vrsti genotipova OV1 * 03, 011v1 * 04 i njihovu kombinaciju, u 3 osobe u 3 osobe Genotip Povezani su sa SD 1 od allela tipa 1: 1 - OOA 1 * 0501, u 2 pacijenta -Oov 1 * 0201. Ukupno 4 od 37 anketiranih je neutralni genotip u odnosu na tip tipa 1.
Distribucija genotipova potomka navedena je u tabeli. 3. U višem "radu napomenuto je da pacijenti sd 1 tipa očeva češće prenose genetsku prelisku
fALSE za dijabetes (posebno, na-01 * 4-genetske vrste) svojoj djeci nego majku. Međutim, studija u Velikoj Britaniji nije potvrdila suštinski utjecaj spola roditelja na predispoziciju jezgre kod djece. U našem radu ne možemo primijetiti takvu regularnost prenosa genetske predispozicije: od pacijenata sa majkama povezanim sa tipom NY-genotipova naslijeđenih 94% djece i od pacijenata sa očevima - 85%.
SD, kao što je poznato, je multigena višefaktička bolest. Kao faktori vanjskog okruženja koji sviraju ulogu okidača, smatra se hranom - potrošnja dojke i rano djetinjstvo proteina kravljeg mlijeka. De
Tabela 3.
Raspodjela genotipova među djecom čiji su roditelji bolesni 1 tip
Gotipovi povezane sa brojem tipa SD 1, koji nisu povezani sa brojem tipa SD 1
0! * U 1 4/4 4 01 * u 1 1/15 1
Ukupno 30 (81%) od samo 7 (19%)
sa novo otkrivenim dijabetesom, postoje povišeni nivoi antitela na protein mlijeka od kravljeg mlijeka, p-laktoglobulin i sranje algumina u odnosu na zdrave sibs, koji se smatraju neovisnim faktorom za SD.
U grupi ispitane djece iz 37 ljudi, samo je 4 bilo na dojenju do 1 godine, 26 ljudi je dobilo majčino mlijeko na 1,5-3 mjeseca, 4 - 6 mjeseci, 3 su bile na mljekarama iz prve sedmice života. Od 5 djece sa pozitivnim antitijelima do P-ćelija 2 su dojele do 6 mjeseci, 3 - do 1,5 - 3 mjeseca; Tada su dobijeni Kefir i mlečne mješavine. Dakle, 89% anketirane djece primilo je proteine \u200b\u200bkravljeg mlijeka u srčanom dob i rano djetinjstvo, koje se mogu smatrati rizičnim faktorom razvoja SD-a u genetski predodređenim osobama.
U ispitivanim porodicama klinički zdravi potomci određeni su citoplazmatskim antitijelima, autoantibode do inzulina i DGC-a. Od 37, anketirano 5 djece bilo je pozitivno na prisustvo antitela u P-ćelije, dok su svih 5 nosioci genetske osjetljivosti na SD (Tabela 4). U 3 od njih (8%) pronađeno je antitijela u DGC, u 1 - do Azoka, u 1 - antitijelima do Azoka
Tabela 4.
Gotipa djece pozitivna na antitijevima K (3 ćelije
Gotype broj pozitivnih antitijela
i inzulin. Dakle, antitijela u Azok imaju 5,4% djece, 2 djece sa pozitivnim antitijelima u DGC su potomci "nuklearnih" porodica. Starost djece u vrijeme otkrivanja antitijela navedena je u tabeli. 5. Da bi se predvidio SD, nivo Azok Titra su od velike važnosti: Što je viši naslov antitela, veća je vjerovatnoća razvoja SD-a, isti se odnosi na antitijele na insulinu. Prema literaturi, visoki nivo antitela u DGC povezani su s sporijim tempom razvoja SD-a (10% u 4 godine) od niskih nivoa (50% u 4 godine), možda zato što su visoki nivoi "antitijela na DGC Navedite "preferirano" aktiviranje humoralnog imuniteta i u manjoj mjeri za aktiviranje ćelijske
Tabela 5.
Starost anketirane djece u trenutku otkrivanja antitijela
Starost anketirane djece (godina) Broj djece pozitivnih na antitijelima
imunitet (tip 1 Tip SD 1 uglavnom je zbog ćelijskog uništavanja P-ćelija od citotoksičnih T-limfocita). Kombinacija različitih antitijela osigurava najoptimalniji nivo predviđanja.
Kod djece sa malim tjelesnim težinama pri rođenju (manje od 2,5 kg), dijabetes se razvija znatno ranije nego kod djece rođene s normalnom masom. Iz podataka anamneze, činjenica da je od 5 djece sa pozitivnim antitijelima 2 rođena s masom tijela više od 4 kg, 2 posto od 2,9 kg.
U direktnim potomcima pacijenata sa pacijentima tip 1, utvrđen je bazalni nivo C-peptida, sav ovaj pokazatelj bio je u okviru normalnog raspona (uključujući djecu sa pozitivnim antitijelima u R-ćelije), studiju nivoa stimuliranog C-peptida nije proveden.
1. Pacijenti vrste tipa 1 u 88,5% slučajeva su nosioci genotipova derivata, OOA1 * 0501, VOV1 * 0201, OV1 * 04, Boa1 * 0301, EOB1 * 0302 ili njihove kombinacije.
2. kod djece iz porodica, u kojima je jedan od uzorka tipa Roditelja 1 tipa, u 89% slučajeva, genetska predispozicija za SD (u prisustvu jednog roditelja pacijenta) i 81% nasljednika u potpunosti povezane sa tipom SD 1 Genotipovi, što im omogućava da ih smatraju grupom vrlo visokog rizika od dijabetesa.
3. Među direktnim potomcima pacijenata sa vrstom SD 1, imajući genetsku predispoziciju, pozitivna antitijela na DGC otkrivena su u 8% slučajeva, ACOC - u 5,4% slučajeva. Ova djeca trebaju dijagnostičku studiju naslona antitijela, Glycohemoglobin i studiju sekrecije inzulina.
* 1 itarite
1. Atkinson M.A., McLaren N.K. // n.engl.j.med.-l 994 -331. P.L 4281436.
2. Aanstoot H.J., Sigurdsson E., Jaffe M. et al // Diabetologia-1994-37.
3. Baekkeskov S., Aanstoot H.J., Christgan S. et al // Priroda-1 990-377.
4. Bain S.C., Rowe B.r., Barnett A.h., Toddj.a. // Diabetes-1994-43 (12). P. 1432-1468.
5. B / NG / Ey P.j., Christie M.r., Bonifacio E., Bonfanti R., Shattock MW Fonte M.T., Bottazzo C.F. // Diabetes-1 994-43. P. 1304-1310.
6. Boehn B.O., Canctus B., Seiblerj. i al // Diabetes-1991-40. Str.1435-1439.
7. Chern M.M., Anderson V.E., Barbosa J. // Diabetes-1982-31. P.L 1 151118.
8. Davies J.L., Kawaguchi Y., Bennett S.T. i dr. // Priroda-1994-371.
9. Erlich H.A., Rotter J.i., Chang J. et al. // Priroda generala.-1993-3. P.358-364.
10. Hahl J., Simell T., Ilonen J., Knip M., Simmel O. // Diabetologia-1 99841. P.79-85.
11. Harrison L.C., Med mene M.c., Deaizpurua H.J. i al // lancet-1993341. P.L 365-1369.
12. Hashimoto L., Habita C., Beresse J.P. i dr. // Priroda-1994-371. Str.161-164.
1 3. Karjalainen J., Martin J.M., Knip M. et al // n.engl.j.med.-L 992-327. Str.302-303.
14. Khan N., Coupert.t., // Dijabetes Care-1994-17. P. 653-656.
15. Landin-Oisson M., Palmer J.P., Lernmark A. Et al // Diabetologia-1992-40. P.L068-1 073.
16. Leslie R.D.C., Atkinson M.A., Notkins A.L. // Diabetologia-1999-42. P.3-14.
17. Levy-Marchal C., Dubois F., Neel M., Tichetj., Czernichow P. // Diabetes-1995-44. Str.1029-1032.
1 8. Lorenzen T., Počiot F., Hougaard P., Nerup J. // Diabetologia-1994-37. Str.321-321.
19. Lorenzen t "Pociot F., Stilgren L. et al // Diabetologia-1998-41. Str.666-673.
20. Nepom G., Erlich H.A. // ann.rev.immunol.-1 991-9. Str.493-525.
21. NerUp J., Mandup-Poulsen T., Molvig J. // Diabetes metab. Rev.-1987-3. P.779-802.
22. Owerbach D., Gabbay K.h. // Diabetes-1995-44.p.l 32-136.
23. Pociotf. U dan.med.bull.-l996-43. P.216-248.
24. REWERS M., Bugawan T.L., Norris J.M., Blair A. Et al. // Diabetologia-1996-39. P.807-812.
25. Rei / Onen H., Ilonen J., Knip N., Akerblom H. // Diabetes-1 991-40.
26. Saukkonen T., Virtaen S.M., Karppinen M. et al // Diabetologia-1998-41. Str.72-78.
27. Schatz D., Krischerj., Horne G. et al // J. Clin. Investirati.-1994-93. P.2403-2407.
28. Spielman R.S., Baker L, Zmijewski C.M. // Ann. Hum. GENET.-1980-44. P. 135-150.
29. Thivolet C., Beaufrere B., Gebuhrer Y., Catelain P., Orgiazzi J. // Diabetologia-1991 -34. P.L86-191.
30. TillIl H., Kobberling J.// Diabetes-1982-36. Str.93-99.
31. toddj.a. U proc. Natl. ACAD. Sci. SAD-1990-377. P.8560-8565.
32. toddj.a., Farral M. // Hum.mol.gen.-5. P.1443-1448.
33. Tuomilehto J., Zimmet P., Mackay I.r. et al // lancet-1994-343.
34. van der Anvera B., Van Waeyenegenge C., Schuit F. et al. // Diabetes-1995-44. P.527-530.
35. Walker A. Gudworth AG. // Diabetes-1980-29. Str.1036-1039.
36. Warram J., Krolewski A., Gottlieb M., Kahn C.r. // n.engl.j.med.-1984-311. Str.149-151.
37. Ziegler A.G., Herskowitz R.D., Jackson R.A. i al // Diabetes Care-1990-13. Str.762-775.




